第Ⅱ相試験後半以降は製薬企業との連携も視野に入れ、最終的には2018年度以降の実用化を目指す。
医薬品の承認を得るための臨床試験(治験)では先ず第Ⅰ相試験で、自由意思に基づき志願した健常成人を対象とし、被験薬を少量から段階的に増量し、被験薬の薬物動態(吸収、分布、代謝、排泄)や安全性(有害事象、副作用)について検討する。
その結果を受け、第Ⅱ相試験では比較的軽度な少数例の患者を対象に、有効性・安全性・薬物動態などの検討を行う。
その後、第III相試験で、実際にその化合物を使用するであろう患者を対象に有効性の検証や安全性の検討を主な目的として、より大きな規模に行う。
肝硬変や脳梗塞などに代表される臓器線維症は、ウィルス感染などで臓器中のある細胞が活性化 してコラーゲンを過剰につくりだし、線維化して硬くなってしまうもので、これまで根本的な治療法がほとんどなかった 。(活性化の原因となる遺伝子に作用する核酸医薬品は見つかっていたが、体内で分解されやすいため、実用化に至っていなかった。)
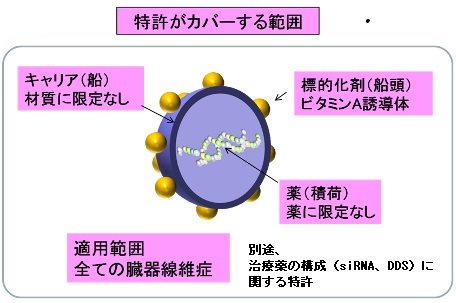
今回の治療は、線維化の原因を選択的に抑えるsiRNA(核酸医薬品の一つ)を薬物として用い、ビタミンA誘導体を標的化剤として患部にのみ選択的に送達するもの(DDS:Drug Delivery System)で、線維症の根本的な治療に繋がる世界初の薬であり、肝硬変のみならず各種の臓器線維症に展開することが可能とされる。
この治療方法に関する基本特許については、日本、中国、豪州、米国、カナダに次いで、欧州と韓国でも取得し、更に治療薬の構成(siRNA、DDS)に関する特許も成立している。
ーーー
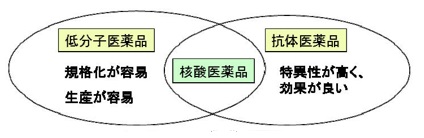
核酸医薬は、DNA(デオキシリボ核酸)やRNA(リボ核酸)の働きを利用して、病気を引き起こす遺伝子やタンパク質に作用するタイプの医薬品で、低分子医薬(化学合成により作られる一般的な医薬品)、抗体医薬に続く、第三世代の医薬品として、近年注目されている。
核酸医薬品は遺伝子にじかに働きかけるため、従来型の医薬品と比べて治療効果が高く、副作用が少ないとされる。
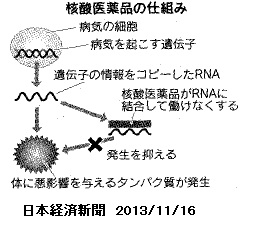
ただし、病気を起こす遺伝子まで到達させるため、体内での安定性やDrug Delivery System(DDS)などの課題を解決する必要がある。今回、日東電工はこれを解決した。
核酸医薬品にはいろいろの種類があり、世界の多くの企業が開発に当たっている。(主としてsiRNAを開発している)
しかし、現状では市販されているのは3品目しかない。
核酸医薬品の原料は、日東電工の米子会社Nitto
Denko Avecia と米 Agilent
Technologiesが合計8割程度の世界シェアを持つ。
2013年11月に住友化学がこれに加わった。
2013/11/28 住友化学、核酸医薬原薬の受託製造開始
ーーー
日東電工は2008年5月から札幌医科大学に下記の研究を行う分子標的探索講座(新津洋司郎
特任教授)を寄付した。
- 臓器線維症(肝硬変、慢性膵炎、腎硬化症、骨髄線維症、肺線維症など)に対するsiRNAHSP47を用いた治療法の開発
- 1.のテーマを発展させ、組織にもともと存在する固有の幹細胞を活性化する再生医療を確立
- がん細胞特にK-ras変異、B-raf変異がん細胞に基づく、新規分子標的薬の開発(合成致死作用を示す薬剤の開発)
- 細胞の運動シグナルを解明する事により、がんの転移や炎症細胞の浸潤を抑制する新薬の開発
その結果、新津特任教授のグループが開発した線維症の治療戦略に、日東電工のキャリア技術を組み合わせ、分子標的DDS(Drug Delivery System)を用いた臓器線維症治療に関する基本特許を、日本・中国・豪州に次いで2012年に米国でも取得した。
この特許は抗線維症薬物を含むキャリア材の表面に、線維症の原因細胞への標的化剤を結合させたDDSとそれを用いた治療に関するものであり、その際、様々な薬物やキャリア材を使用することが可能である。
分子標的DDSは、病気の原因となる細胞にのみ直接薬物を届けるシステムで、従来治療が困難な疾患に対し、副作用が少なく高い治療効果を期待できる。
今後は、臓器線維症をはじめとする難治性疾患の治療薬に取り組む。
ーーー
日東電工は2011年2月に、今後成長が期待される核酸医薬の分野において事業基盤の強化を目的に、米国マサチューセッツ州にある核酸医薬の製造受託分野でトップのAvecia Biotechnologyを買収した。(→Nitto Denko Avecia Inc.)
Avecia Biotechnologyは、核酸医薬の製造受託分野でトップシェアを誇り、前臨床段階から商業的製造までのステージにおいて、 世界最大のcGMP製造能力をベースに、分析方法開発、プロセスバリデーション、安定性試験、品質管理及び薬事面サポートと幅広いサービスを提供している。
日東電工は2012年11月、Nitto Denko Aveciaを通して、 核酸医薬の分野において更なる事業拡大を目的に、核酸医薬の受託製造において主要な製薬会社やバイオテック会社へのサービス提供の経験を有し、またRI標識能力及び有機合成能力を有するGirindus America Incと資産買収契約を締結した。
コメントする