理研と住友化学は2月19日、共同研究グループが、ヒトES細胞(胚性幹細胞)から、毛様体縁幹細胞ニッチ(幹細胞を長期間維持できる特別な微小環境)を含む立体網膜(複合網膜組織)を作製することに成功したと発表した。
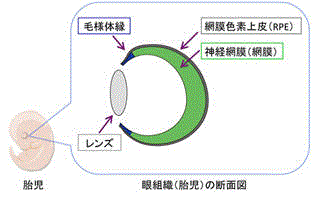
毛様体縁は、胎児の網膜の端に存在する領域で、ヒトの毛様体縁の網膜発生における役割はほとんど明らかにされておらず、これを解明するには、ヒト毛様体縁を含む立体的な網膜を安定的に作製する新たな技術が有用である。
これまで理研では、亡くなった笹井芳樹博士を中心に 「SFEBq法(無血清凝集浮遊培養法)」という分化誘導法を開発し、ES細胞やiPS細胞から、 大脳、視床下部、下垂体、小脳や網膜などの複雑な神経組織を作製しており、網膜についても、マウスES細胞やヒトES細胞から立体網膜を作製している。
しかし、この方法では、分化を促進するために、培養液中に動物由来の基底膜抽出物を添加していた。
この基底膜抽出物は、マウス肉腫由来細胞の抽出物であり、さまざまな成分を含んでいるため品質保証が難しく、再生医療用途には
向いていない。
今回、理研と住友化学の共同研究グループは、この技術をさらに改良して、新しい網膜分化誘導法の開発に 成功した。
概略は下記の通り。
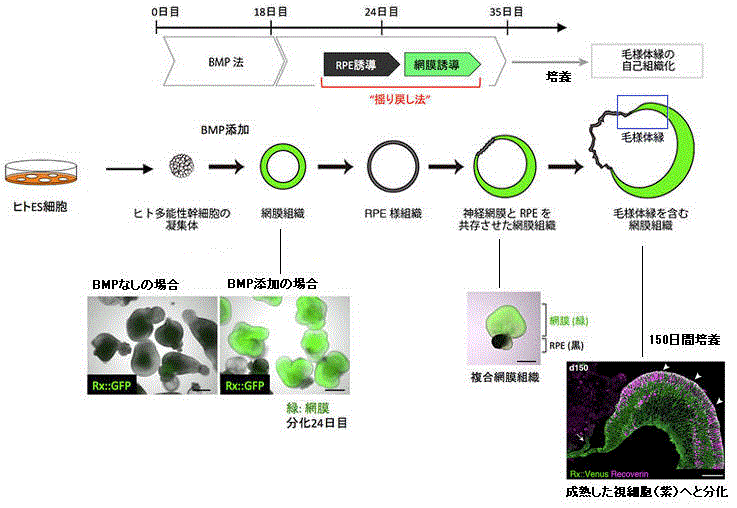
1)選択的な網膜分化誘導法(BMP法)の開発
SFEBq法では分化を促進するために、培養液中に動物由来の基底膜抽出物を添加していた。
今回は、基底膜抽出物を使わず、分化培養の初期に BMP (Bone Morphogenetic Protein:骨形成タンパク質)と呼ばれるシグナル作用物質を添加することで、ヒトES細胞から効率よく網膜組織へと分化誘導できることを発見した。
BMP法は、基底膜抽出物を使った従来法(効率は最高でも70%で、不安定)と比べ、分化誘導効率が80%程度と高く、かつ安定している。
2)毛様体縁を持つ網膜組織の作製法(揺り戻し法)の開発
毛様体縁は、胎児期の網膜(神経網膜)と網膜色素上皮(RPE)の境界領域に形成される。
これまでの研究により神経網膜の分化・維持にはFGFシグナルが、また RPEの分化・維持にはWntシグナルが重要な役割をしていることが分かっている。
共同研究グループは、ヒトES細胞からBMP法で作製した網膜組織を、まずFGFシグナルの阻害薬とWntシグナルの作動薬を含む培養液で培養してRPEへと分化させ、その後、再び神経網膜を誘導する条件で培養することにより神経網膜へと戻すことで(「揺り戻し」)、神経網膜とRPEが共存した複合網膜組織の形成に成功した。
これまでの方法では、神経網膜のみ、または、RPEのみを作ることはできていたが、神経網膜とRPEが共存する複合網膜組織を、効率よく安定的に作るのは困難だった。
今回、複合網膜組織を安定して40%程度の効率で作製できるようになった。
3) 培養
この毛様体縁を含む複合網膜組織は、60日目まで培養を続けると、幼若な視細胞前駆細胞を豊富に含むことが確認された。
この複合網膜組織を解析したところ、神経網膜とRPEの境界領域に胎児の毛様体縁によく似た特徴を持つ組織が形成された。
このことは、ヒトES細胞から神経網膜とRPEを同時に誘導することで、自己組織化により、両者の境界領域に毛様体縁が形成されることを示唆する。
さらに、150日目まで培養を続けると、分化の進んだ視細胞が産生された。
毛様体縁を含む立体網膜を詳しく解析したところ、毛様体縁に幹細胞が豊富に含まれることが分かった。
また、毛様体縁に含まれる幹細胞は、光を受ける視細胞や、脳に視覚情報を伝える神経節細胞への分化能を持つことも確認した。
さらに、毛様体縁の近くで立体網膜を成長させる細胞が供給されることを発見した。
これらの結果から、ヒト毛様体縁には幹細胞が存在し、この幹細胞が増殖する機能を発揮することで、網膜を試験管内で成長させることが分かった。
ヒト立体網膜を用いた再生医療を広く普及させるための大きな課題の1つとして安定生産が難しいという課題があったが、本研究により、安定生産に適した分化誘導技術を確立できた。
この技術の長所は、
(1)分化誘導効率が安定的に高い点、
(2)複合網膜組織は品質のバラツキが小さい点(網膜の形状、神経網膜とRPEの比率)、
(3)複合網膜組織の毛様体縁付近は、胎児網膜と良く似た規則的な立体構造(連続上皮構造)をとる点、
が挙げられる。
現在、理研多細胞システム形成研究センター網膜再生医療研究開発プロジェクトの高橋政代プロジェクトリーダーらは、住友化学子会社の大日本住友製薬との共同で、本研究成果をヒトiPS細胞に適用して、網膜色素変性を対象とした再生医療の実現に向けた研究開発を進めている。
ーーー
大日本住友製薬と理研認定ベンチャーのヘリオス(旧称 日本網膜研究所)は2013年12月に再生・細胞医薬事業に関する提携を発表、2014年2月にJV サイレジェンを設立した。
ヘリオスはiPS細胞から生体内のRPE細胞と同じ形態と機能を持つRPE細胞を分化誘導することに成功しているが、これを拡大培養し、RPEの懸濁液及びシートを作成し、それぞれドライ型、ウェット型の治療に使用しようというもの。
理化学研究所の高橋政代プロジェクトリーダーは、iPS細胞を使い、滲出型加齢黄斑変性の患者を対象に、目の網膜を再生する世界初の臨床研究を実施しているが、ヘリオスがシートの作成を担当している。
2013/12/4 大日本住友製薬と理研認定ベンチャーのヘリオス、iPS細胞由来医薬品を共同開発
コメントする