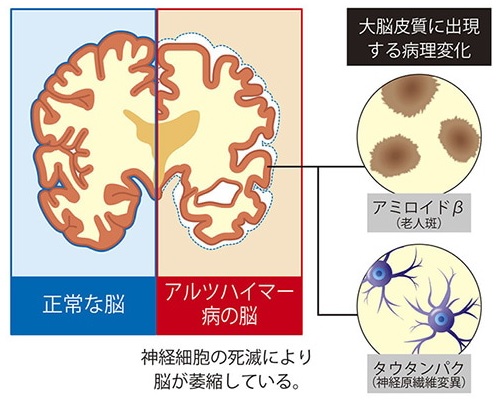
アルツハイマー型認知症の原因は未だ解明されていないが、進行に伴っていくつかの特有の病変が見られる。例えば、神経細胞の外側では「アミロイドβ」が蓄積して老人班を形成し、神経細胞の中では「タウタンパク」が蓄積してタンパク質が糸くず状に変化したようなもの(神経原繊維変化)が見られるようになる。
2021/6/25 島津製作所、少量の採血でアルツハイマー病の原因候補物質を測定
1.現在のアルツハイマー治療薬
アルツハイマーは、病理学的には神経原線維変化とアミロイドβ沈着の2つを特徴とする変化により、脳の神経細胞死が生じ、記憶力低下をはじめとする認知機能障害が緩徐に進行する病気。
現時点で認可されているアルツハイマー病の治療薬は以下の4つで、いずれも根治を目的としたものではなく、進行を少し(半年〜1年程度)遅らせるものでしかない。
いずれも、ニューロン間の情報を伝達する化学物質である神経伝達物質を制御することにより機能する。
①アリセプト®(ドネペジル)
②レミニール®(ガランタミン)
③リバスタッチ®、イクセロン®(リバスチグミン)
いずれも、アセチルコリンエステラーゼ阻害薬で、脳内で記憶保持や集中、覚醒などの作用がある神経伝達物質のアセチルコリンの分解を抑制し、脳内の相対的濃度を高めることで、アルツハイマー型認知症やレビー小体型認知症の中核症状の進行を抑制する。
軽度~中等度の段階を中心に幅広く服用されている。
④メマリー®(メマンチン) NMDA受容体拮抗剤
グルタミン酸は脳内の興奮性の神経伝達物質で、この作用を弱めることで、過剰な興奮による脳神経の損傷を抑え、中核症状の進行を抑制する。
比較的重度の認知症にも用いられる。
NMDA受容体拮抗剤とアセチルコリンエステラーゼ阻害剤とは効果をもたらすしくみが異なるため、これらが併用されることもあ る。
2.新薬開発(アミロイドβ仮説)
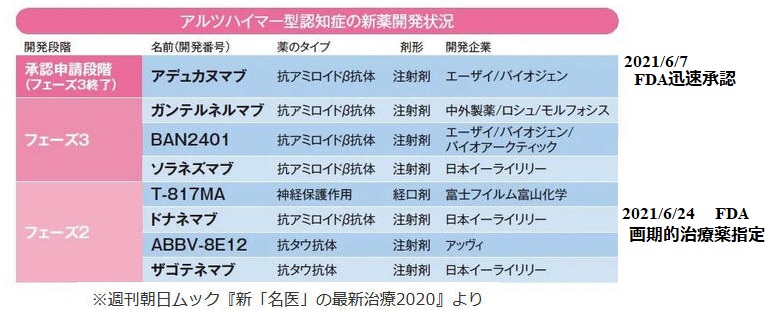
注) 一般名の末尾の「マブ」はモノクローナル抗体医薬の意味。
末尾の「ビル」は抗ウイルス薬、「ニブ」は キナーゼ阻害薬
「Aβ(アミロイドβ)仮説」
脳の神経細胞外にAβが蓄積→タウ蛋白のリン酸化→神経原線維変化→細胞毒性が生じ、神経細胞が死滅→認知症を発症
抗Aβ抗体:Aβを除去
抗タウ抗体:タウを除去したり、タウの凝集を阻害
T-817MA:神経細胞保護効果や神経突起伸展促進効果のあるT-817MA投与で、リン酸化タウの減少を確認。
①エーザイ/バイオジェン ADUHELM(一般名:アデュカヌマブ)
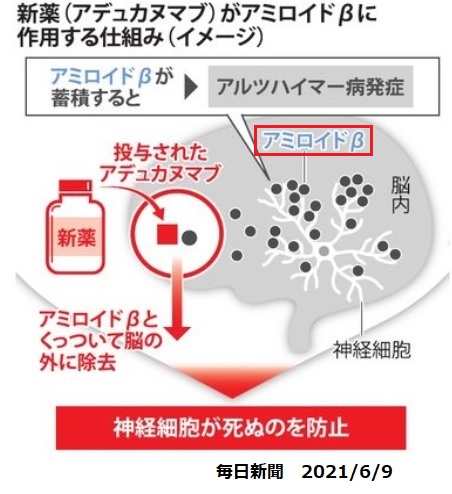
米食品医薬品局(FDA)は2021年6月7日、エーザイと米バイオジェンが共同で開発するアルツハイマー型認知症治療薬候補ADUHELM(一般名:アデュカヌマブ)について、脳内のアミロイドβプラークを減少させることにより、アルツハイマー病の病理に作用する初めてかつ唯一の治療薬として、迅速承認(accelerated approval)したと発表した。従来の認知症薬とは異なり、認知機能の低下を長期的に抑制する機能を持つとして世界で初めて承認された。
アミロイド斑(プラーク)は、アミロイドβ蛋白が蓄積したもので、アルツハイマー病患者の脳にみられる。新薬はこのレベルを下げるもの。
2021/6/8 エーザイとバイオジェンのアルツハイマー新薬、米で承認
ADHUHELMについては、2020年11月7日のFDAの末梢・中枢神経系薬物諮問委員会で、有効性に対して否定的な見解が出された。
賛成 反対 保留 アルツハイマー病治療としての有効性に関する説得力のあるエビデンスを示しているか 1 8 2 試験がアデュカヌマブの有効性の裏付けとなるエビデンスを示しているか 0 7 4 アデュカヌマブの薬力学的効果に関して説得力のあるエビデンスを示しているか 5 0 6 302試験をアデュカヌマブのアルツハイマー病に対する有効性に関する主要なエビデンスとみなすことができるか 0 10 1
FDA諮問委員会の提言は、FDAによる審査において考慮されるが、拘束力はない。しかし、提言に反する承認は異例。2019/10/24 Biogenとエーザイ、一旦治験中止したアルツハイマー薬の承認申請へ今回の承認をめぐり、委員会のメンバーのうち、反対票を投じた大学の神経学者と、当日の採決に加わらなかった医療機関に勤める人物の2人が辞任した。委員会の反対にもかかわらずFDAが、条件付きで承認したことへの抗議だという。
このため、FDAのウッドコック長官代行は、承認に至るまでのバイオジェンとFDAとのやりとりが適正だったか調査するよう、米厚生省の監査部門に調査を要求、監査部門は8月4日、承認過程を調査すると表明した。
米下院の二つの委員会も、同薬の承認をめぐる調査に着手した。一方、二つの米大手医療機関は、当面は患者に使用しない方針を表明した。
② Ely Lilly 「ドナネマブ」
Ely Lilly は2021年6月24日、同社がアルツハイマー病に対して開発中の抗体医薬品であるdonanemabがFDAから画期的治療薬指定(Breakthrough Therapy designation)を受けたと発表した。
画期的治療薬指定は、重篤な疾患の治療を目的として、FDAの承認を受けている既存の医薬品と比較して、当該医薬品が臨床的に意義のある評価項目を大幅に改善する可能性が臨床的エビデンスにより示された場合、その開発と審査の迅速化を図ることを目的としている。
今年後半に迅速承認制度に則り donanemabの生物学的製剤承認申請書(BLA)を提出する予定
Aβペプチドは脳内に沈着し、過剰になると互いに結合してタンパク質プラークを形成する。
ドナネマブは、このタンパク質プラークを標的とし、脳内で負担となる余分なタンパク質を除去する。
(単に新しいプラークの沈着または既存のプラークの成長を防ぐのではなく、沈着したプラーク自体を標的にすることが、脳から既存のアミロイド負荷を取り除くために必要)以前のプラーク結合抗体のいくつかは、脳に微小出血を引き起こしたために放棄されたが、これは微小出血を引き起こすことなくマウスのプラークを除去することが報告されている。
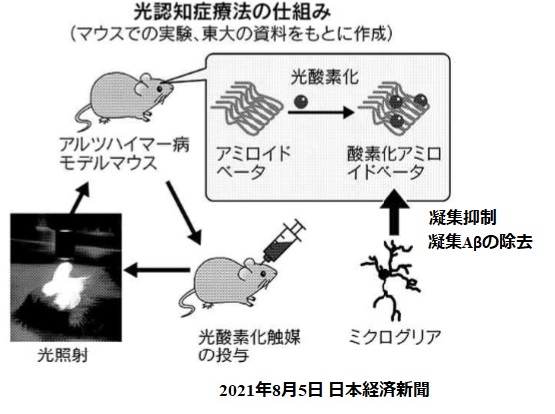
3.光認知症療法
東京大学は2021年4月、光酸素化法を開発したと発表した。
脳内でアミロイドβペプチド(Aβ)が凝集・蓄積することがAD発症の原因と示唆されており、Aβの凝集を抑制すること 、また凝集したAβを効率よく除去することがAD根本治療戦略として考えられている。
今回、光照射と光酸素化触媒を用いた光酸素化法を確立した。
・ 凝集Aβ除去には脳内免疫担当細胞であるミクログリアが関与していることを確認。
・ 光照射と、光によってアミロイド選択的な酸素化活性をもつ低分子化合物である光酸素化触媒を用い、
アミロイドに対して酸素を付加する。
・ 光酸素化された凝集Aβは凝集がほぐれた状態になり、ミクログリア細胞内のリソソーム分解酵素による分解が亢進する。
・ 患者脳内に蓄積したAβに対しても光酸素化が可能である。
凝集Aβに対する光酸素化が、さらなる凝集抑制効果と凝集Aβの除去という2つの効果を有し、AD根本治療戦略となりうる可能性を示した。

コメントする