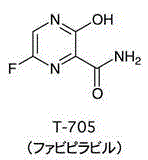
台湾の感染症対策を行う衛生福利部疾病管制署(台湾CDC)はこのたび、抗インフルエンザウイルス薬「アビガン®錠200mg」(Favipiravir)
を備蓄することを決定した。
これを受け、富士フィルムは7 月13 日に同署へ「アビガン錠」を供給した。
今回の備蓄は、台湾でヒトへの感染の危険性が高まっている鳥・豚インフルエンザおよび新型インフルエンザの治療薬として台湾国民のリスクに備えるもので、「アビガン錠」は現時点では台湾CDCから製造販売承認されてはいないが、台湾CDC は「アビガン錠」の持つ新しい作用メカニズムなどを評価し、「アビガン錠」の特例輸入を決定した。
「アビガン錠」はヒトが鳥・豚インフルエンザや新型インフルエンザに感染した時に使用され、また実際投与された場合には、その情報が富士フイルムに提供される。
今回の供給は、台湾CDC から「アビガン錠」の輸入委託を受けた、現地製薬大手の生達化学製薬を通じて行った。今後、富士フイルムは、同社と提携し、台湾での製造販売承認の早期取得を目指す。
ーーー
ファビピラビルは富士フイルム傘下の富山化学工業 (富士フイルム 66%、大正製薬 34% 出資)によって1998年に発見された。
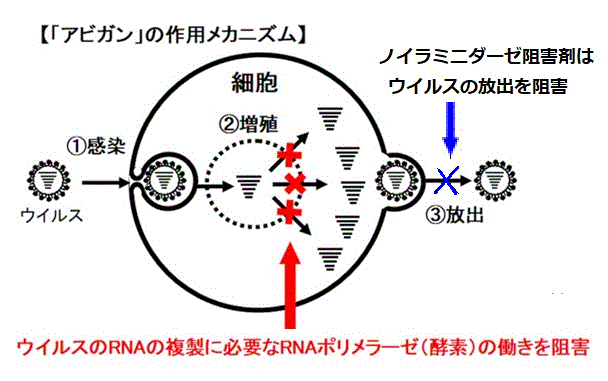
インフルエンザウイルスは、感染した細胞内で遺伝子を複製し、増殖・放出することで他の細胞に感染を拡大する。
現在、治療に用いられている抗ウイルス剤はノイラミニダーゼ阻害剤(Neuraminidase inhibitors)で、増殖されたウイルスの放出を阻害して感染の拡大を防ぐものだが、アビガンは、ウイルスの細胞内での遺伝子複製を阻害することで増殖を防ぐRNAポリメラーゼ阻害剤である。
鳥インフルエンザウイルスA(H5N1)及び A(H7N9)等に対する抗ウイルス作用が期待されており、実験動物レベルでは既に効果が確認されている。
富山化学工業は2014年3月24日、日本で錠剤タイプの新しい抗インフルエンザウイルス薬「アビガン®錠200mg」の製造販売承認を取得した。アビガンは、新型又は再興型インフルエンザウイルス感染症が発生し、既存の抗インフルエンザ薬が無効又は効果不十分である場合に備え、新しいメカニズムのアビガンを使用可能な状況にしておくことは意義があると判断され、世界に先駆けて国内で承認となった。
直ちに医家向けに販売するのではなく、厚生労働大臣から要請を受けて製造・供給等を行うもので、新型又は再興型インフルエンザウイルス感染症が発生し、本剤を当該インフルエンザウイルスへの対策に使用すると国が判断した場合に、患者への投与が検討される。
承認には次のような厳しい条件がついている。
・動物実験で初期胚の致死及び催奇形性が確認されていることから、妊婦または妊娠している可能性のある婦人には投与しないこと。
・日本人を対象にした薬物動態試験と追加臨床試験結果を医薬品医療機器総合機構に提出し、成績が確認されるまでは「原則製造禁止」 。
(申請に用いたのが米国の試験結果で、日本人を対象にしたものがなかった。)
但し、パンデミック時など厚労相が「要請」した際は製造できる。
ーーー
WHOは2014年8月、エボラ出血熱の患者が過去最大の規模で増え続けている事態を受け、安全性などが最終的に確認されていない未承認の薬の使用を一定の条件の下で認める方針を明らかにした。
ファビピラビルは既にインフルエンザ感染者の抗ウイルス剤として治験が重ねられており、エボラ出血熱の治療に適用する上で優位性がある。
富士フイルムは2014年9月26日、「アビガン®
錠200mg」が、エボラ出血熱に罹患した患者の治療のため、フランスの病院で投与されたと発表した。
「アビガン錠」を含む3剤を服用していたエボラ出血熱によるフランス人女性患者は10月4日に無事退院した。
韓国保健福祉部は2014年10月30日、「富士フイルムとの間でエボラ治療剤アビガンの供給について合意した」と明らかにした。
ギニア南東部の治療センターでアビガンの臨床試験を行っている国際医療活動連盟(ALIMA)は、血中のウイルス量が低・中レベルの患者では、死亡率が30%から15%に低下したと発表した。ただ、ウイルス量が多ければ効果はみられないという。
富士フイルムHDの古森重隆・会長兼CEOは2015年2月27日、アビガンにはこれまでに約20カ国が関心を示し、大量の注文に応じる用意ができていると述べた。
コメントする