武田薬品工業は1月9日、米ナスダック上場でがん治療薬を手がける製薬会社、ARIAD Pharmaceuticals, Inc を約54億ドルで買収すると発表した。
TOBを実施し、完全子会社にする。
ARIADは血液がんの一種である慢性骨髄性白血病(「CML」)およびフィラデルフィア染色体陽性急性リンパ性白血病(「Ph+ ALL」)の治療薬Iclusig®(一般名:ponatinib)を発売済みで、この薬は2016年12月期に1億8千万ドル程度の売り上げを見込む。非小細胞肺がんを対象とした薬も臨床試験を実施中で、将来は年10億ドル超の売上高を期待できるという。
後記の通り、大塚製薬 が日本を含むアジア10カ国・地域において、本剤の共同開発・商業化の権利を取得している。
もう一つの薬 brigatinibは2017年前半に米国での承認取得を見込んでおり、ベスト・イン・クラスのALK 阻害薬(肺がんの遺伝子変異の治療)となる可能性がある。
武田薬品は消化器系疾患領域、オンコロジー(癌)、中枢神経系疾患領域の3分野(+ワクチン)を重点領域とし、これらの分野に経営資源を投じるため、事業の選択と集中を進めている。今回の買収で、グローバルなオンコロジー(がん)ポートフォリオをさらに拡大する。
ーーー
武田薬品は2008年4月に、米国バイオ医薬品会社 Millennium Pharmaceuticals, Inc.を約88億ドルで買収することを発表した。
同社は5月9日、91.9%の応募を受け、本TOBが成立したと発表した。
癌領域におけるリーディングカンパニーで、癌領域および炎症疾患領域において有望なパイプラインを保有する。
2011年5月19日、スイスのチューリッヒに本社を置く非上場製薬会社Nycomed A/S を買収すると発表した。
同年9月30日に買収を完了し、同日をもって100%子会社とした。
2011/5/23 武田薬品、Nycomed社を買収
2014年6月にGlaxoSmithKline 出身のChristophe Weber を代表取締役社長とし、翌年CEOになった。
その後同社は、重点領域の消化器系疾患領域、オンコロジー(癌)、中枢神経系疾患領域の3分野(+ワクチン)に経営資源を投じるため、事業の選択と集中を進めている。
2015年12月16日、呼吸器系疾患領域事業をAstraZenecaに5億7500万ドルで売却することで合意した。2015/12/22 AstraZeneca、買収による事業拡大
2015年11月30日、後発薬世界最大手のイスラエルのTeva Pharmaceutical と、日本で両社によるジェネリック医薬品の合弁会社を設立する基本合意契約を締結した。
武田薬品は長期収載品事業を分割し、ジェネリック医薬品事業を営む大正薬品に承継、大正薬品は武田テバ薬品と改称する。2015/12/28 武田薬品とTeva Pharmaceutical の日本の合弁会社の概要
武田薬品は2016年12月15日、子会社で試薬大手の和光純薬工業を富士フィルムに売却する契約を締結した。
2016/12/22 富士フィルム、和光純薬を買収
武田薬品は2016年10月11日、がん領域における強力で非常に特徴的な抗体薬物複合体のHumabody® 製剤での創出・開発を行うバイオ医薬品会社の英国のCrescendo Biologics Limited との間で、この技術を使ったがん治療薬の創製、開発および販売に関して、グローバルでの戦略的提携およびライセンス契約を締結した。
2016/10/14 武田薬品、がん治療薬開発で英 Crescendo と提携
ーーー
ARIADが既に販売しているIclusig®(一般名:ponatinib)は、慢性骨髄性白血病(「CML」)およびフィラデルフィア染色体陽性急性リンパ性白血病(「Ph+ ALL」)の治療薬である。
CMLやPh+ALLでは、22番染色体 のbcr 遺伝子という領域と9番染色体のabl 遺伝子という領域での転座によって、これらの遺伝子が繋がり、bcr-abl という新しい遺伝子領域ができる。
この結果、Bcr-Abl という異常なタンパクが作られるようになり、このタンパクの作用によってシグナル伝達の異常が発生し、白血病細胞の過剰な増殖が起こる。日本ではCMLは10万人に1人程度の割合ですべての年齢層で発症する。患者数は約11,000人と推定されている。
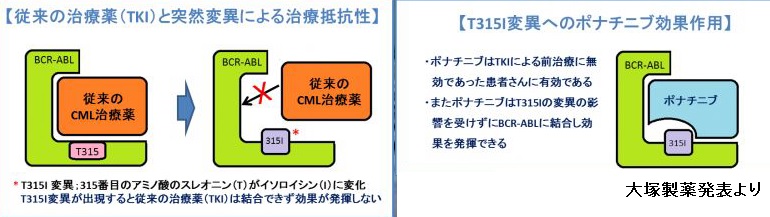
従来の治療薬の場合、Bcr-Abl タンパクに突然変異が起こり、抵抗性が発生するが、Iclusigの場合はそれらにも効果がある。
2012年12月に米国FDAで承認され、2013年7月に欧州でも承認を取得した。
大塚製薬は2014年12月に日本、インドネシア、マレーシア、中国(香港含む)、フィリピン、シンガポール、韓国、台湾、タイ、ベトナムのアジア10カ国・地域において、Iclusig の共同開発・商業化の権利を取得した。
2016年1月に日本でCMLとPh+ALLの新規経口治療薬として申請を行い、2016年9月28日に「アイクルシグ®錠15mg(一般名:ポナチニブ塩酸塩)」の国内における製造販売承認を取得した。
日本で2015年9月にオーファンドラッグとしての指定を受けている。
韓国および台湾では現在審査中。
コメントする