大塚製薬と米国の Proteus Digital Health は11月13日、世界初のデジタル錠剤「エビリファイ マイサイト (Abilify MyCite®)」の承認を米国FDAから取得したと発表した。
大塚製薬によると、このような医薬品と医療機器を一体化した製品の承認は世界初という。
「エビリファイ マイサイト」は、 抗精神病薬のエビリファイの錠剤に摂取可能な約3mmの極小センサー Ingestible Event Marker sensor を組み込んだもので、同剤の適応である成人の統合失調症、双極性Ⅰ型障害の躁病および混合型症状の急性期、大うつ病性障害の補助療法において使用され る。
この錠剤を服用するとセンサーが胃内でシグナルを発し、患者の身体に貼り付けたシグナル検出器「MYCITE Patch」がそれを検出する。
この検出器は、患者の服薬データだけでなく、活動状況などのデータを記録し、専用のアプリケーション「MYCITE APP」を備えたスマホなどに送信する。
アプリには、睡眠や気分などを患者が入力することもできる。
これらのデータはスマートフォンなどのモバイル端末に転送され、患者の同意があれば医療従事者や介護者との情報共有も可能にな る。
医師の処方通りに患者が薬を飲んだかどうかを第三者が確認でき、効果的な治療ができ、医療費の削減にもつながると期待される。
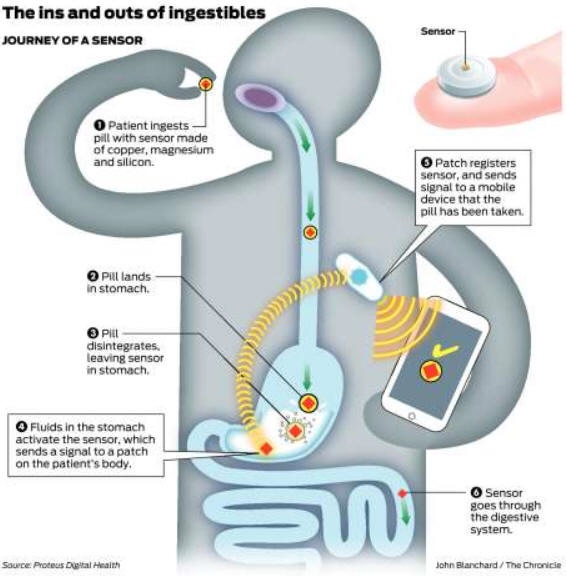 |
① センサー入りの薬を飲む。
② 錠剤が胃に到着
③ 薬が溶け、センサーが胃に残る。
④ センサーが胃液に反応、身体に貼り付けたMYCITE Patchに信号を転送。
⑤ MYCITE Patchがスマホなどに いつ薬が飲まれたかを送信
⑥ センサーは排泄される。
米国内の試算では、処方通りに薬を飲まなかったことで病気が悪化したり、別の治療が必要になったりして年間に計1千億ドルのコストがかかっているという。
一方、 患者の様子を遠くから監視することにもつながりかねないとの懸念があり、患者のデータ管理や利用にはより慎重さを求める声が上がる。
両社は、このシステムにより、服薬や活動の状況を把握できることで、患者と介護者および医療者のコミュニケーションを促進し、それぞれの患者により適した治療の選択に寄与 するとしている。
米国において、まずは少数の患者の使用経験を通じ、製品の価値を確認していくとしている。日本での販売は現在予定していない。
コメントする