厚労省は6月2日、新型コロナウイルスのワクチンを早期実用化する「加速並行プラン」をまとめた。
国内外で研究開発が進むワクチンについて国内で「2021年前半に接種開始」との目標を設定 した。
ワクチン開発は通常、基礎研究→臨床試験→薬事申請・生産体制整備→薬事承認・生産開始と、実用化に数年を要する。
「加速並行プラン」では、臨床試験の段階で民間のリスクを政府が負担し、資金を投入して生産体制整備に着手する。審査・承認の過程も大幅に短縮する。
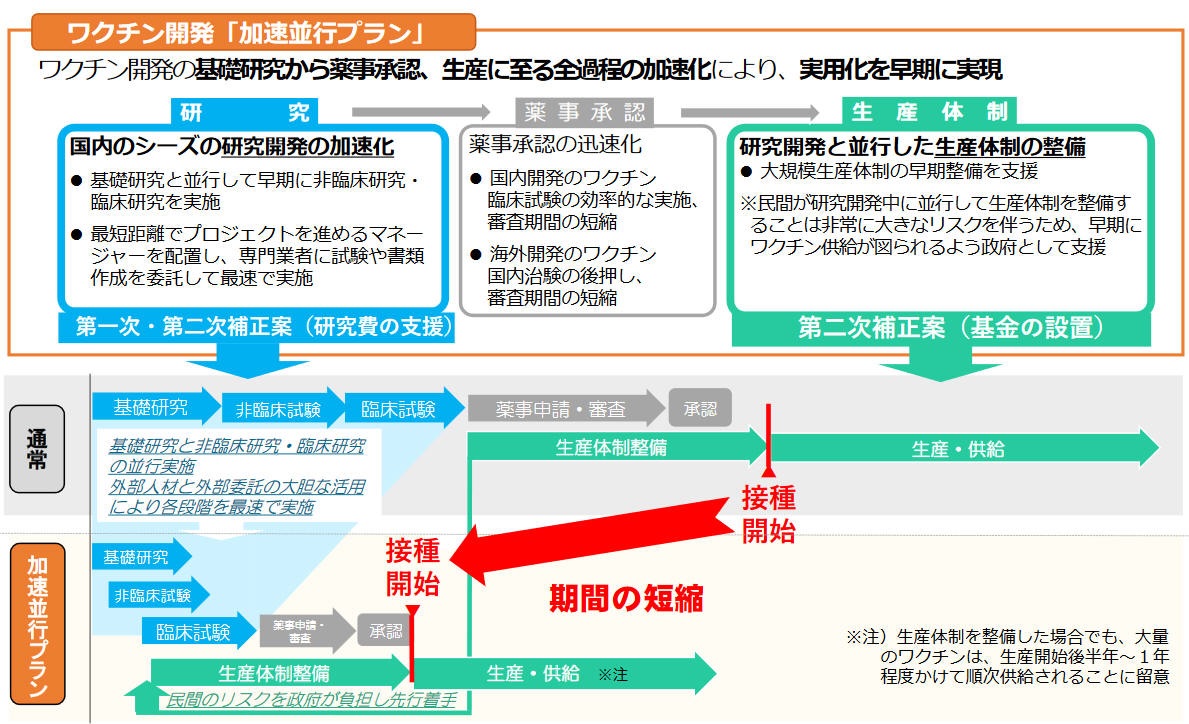
但し、この場合でも、大量供給できるまでには「生産開始後半年~1年程度」かかるとしている。国内で「2021年前半に接種開始」との目標を設定しているが、実際には、出来たとしてもごく一部にとどまると思われる。
政府は今年度第2次補正予算案で製造ラインの整備費を基金化し約1400億円を計上し、1件200億~300億円をめどに5件程度を公募で選定する。
厚生労働省は2日、新型コロナウイルスのワクチンを早期実用化する「加速並行プラン」をまとめた。国内外で研究開発が進むワクチンについて国内で「2021年前半に接種開始」との目標を設定。最終的に国民全員に接種することを念頭に、国費を投じて製造ラインを整備するとした。
公明党が国会内で開いたプロジェクトチームで示した。ワクチン開発は通常、基礎研究▽安全性の確認を含めた薬事承認▽生産――と、実用化に数年を要する。通常は臨床試験が終わり実用化のめどが立ってから着手する製造ラインの整備について、プランは研究中から政府が資金を投入し、審査・承認の過程も大幅に短縮するとした。一方でワクチンの生産体制が整った後も、大量供給できるまでには「生産開始後半年~1年程度」かかるとした。
政府は今年度第2次補正予算案で製造ラインの整備費を基金化し約1400億円を計上。補正予算の成立後、1件200億~300億円をめどに5件程度を公募で選定する。
ーーー
既報の通り、WHOによると臨床試験段階にあるものは10件だが、日本のものは含まれていない。
厚労省によると、日本医療研究開発機構(AMED)が支援しているワクチン開発状況は以下のとおり。
| 基本情報 | 取り組み状況 | 目標と対応 | 生産体制の見通し | |
| 組換えタンパクワクチン (感染研/UMNフ ァーマ/塩野義) |
遺伝子組換え技術を用いて培養細胞によりコロナウイルスのタンパク質(抗原)を製造し、コロナウイルスタンパク質(抗原)を人に投与するための注射剤。 | ○ワクチンの候補を作製中 ○動物を用いた有効性評価を開始予定 |
有効なワクチン候補を選定し、その後、非臨床試験及び臨床試験の実施を目指す。 | 塩野義が開発主体 |
| mRNAワクチン (東大医科研/第一三共) |
メッセンジャーRNAを人に投与する注射剤。 人体の中で、コロナウイルスのタンパク質(抗原)が合成され、免疫が誘導される。 |
○ワクチンの候補の作製が終了 ○動物を用いた有効性評価を実施中 |
有効なワクチン候補を選定し、その後、非臨床試験及び臨床試験の実施を目指す。 | |
| DNAワクチン (阪大/アンジェス/タカラバイオ) |
DNAを人に投与する注射剤。 人体の中で、DNAからmRNAを介して、コロナウイルスのタンパク質(抗原)が合成され、免疫が誘導される。 |
○ワクチンの候補の作製が終了 ○動物を用いた有効性評価を実施中 |
最短で7月から臨床試験開始の意向。 | タカラバイオが生産予定 |
| 不活化ワクチン (KMバイオロジクス/東大医科研/感染研/基盤研) |
不活化したコロナウイルスを人に投与する従来型のワクチン。 | ○コロナウイルスが増殖するかを確認中 | 2020年度中に非臨床試験終了を目指す。 | |
| ウイルスベクターワクチン (IDファーマ/感染研) |
コロナウイルスの遺伝情報を持ったセンダイウイルスを投与するワクチン。人体の中でコロナウイルスのタンパク質(抗原)が合成される。 | ○動物を用いた有効性評価を開始予定 | 最短で9月から臨床試験開始の意向。 |
2020/5/22 アンジェスの新型コロナウィルス向けDNA ワクチン開発
※このほかAMEDで、基礎研究段階の開発を支援(新潟大・東京都医学総合研究所・慶応大・東大・長崎大)
海外での開発で、日本政府がCEPI(感染症流行対策イノベーション連合)に資金を拠出し、CEPIが支援しているワクチン開発主体は以下のとおり。
これらについて、日本で早期に生産できるのかどうか不明。
| ワクチンの種類 | CEPIが支援する開発主体と状況 | |
| 抗原を注射して免疫を付けるタイプ | 組換えタンパクワクチン | Novavax社(米)第1/2相臨床試験を開始。 Novavaxは、専有のナノ粒子技術を適用して作製したCOVID-19のワクチン候補(NVX-CoV2373)に関する第1/2相臨床試験を5月20日に開始したと発表した。 同試験は、CEPIから3億8800万ドルの資金を得て行われている。 |
| Clover Biopharmaceuticals Australia(豪)「2か月以内に豪での第1相臨床試験の被験者募集を開始したい」としている。 | ||
| ペプチドワクチン | Queensland大学(豪)/GSK社(英) | |
| 遺伝子を注射して、人体がコロナウイルスの抗原をつくり、免疫をつけるタイプ | m-RNAワクチン | Moderna社(米)/国立アレルギー感染症研究所(米):第1相臨床試験の中間結果を公表。第2相臨床試験を2020年5月、第3相臨床試験を2020年初夏に開始予定。ロンザ社(スイス)と提携。 2020/5/19 米Moderna、新型コロナウイルスワクチン治験で抗体確認 |
| CureVac社(独) | ||
| DNAワクチン | InovioPharmaceuticals社(米)第1相臨床試験を開始。 INOVIOとGeneOne Life Scienceは4月29日、DNAワクチンINO-4700(Spike糖タンパク質を標的にするDNAワクチン)の第1/2a相試験12週の中間データを発表した。 |
|
| ウイルスベクター | オックスフォード大(英):第1相臨床試験を完了(結果は未公表)。第2/3相臨床試験を開始。アストラゼネカと提携。 2020/5/22 アストラゼネカ、新型コロナウイルスのワクチン 9月に供給へ |
|
| 香港大学(中) | ||
| パスツール研究所(仏)/テーミス社(墺:MSD社の子会社)/ピッツバーグ大学(米) | ||
※CEPI (Coalition for Epidemic Preparedness Innovations) とは、世界連携でワクチン開発を促進するため、2017年1月ダボス会議において発足した官民連携パートナーシップ。日本、ノルウェー、ドイツ、英国、オーストラリア、カナダ、ベルギー政府が関わる。
コメントする