WHOはCOVID-19 治療薬のremdesivirについて、世界各地の臨床試験を分析した結果、「死亡率の低下などにつながる重要な効果はなかった」として、 「症状の軽い重いにかかわらず、入院患者への投与は勧められない」とする指針を公表した。
死亡率の低下や人工呼吸器の必要性、それに症状の改善にかかる時間について「重要な効果はなかった」とし 、「症状の軽い重いにかかわらず、入院患者への投与は勧められない」としている。
WHOに勧告する専門家のパネル WHO Guideline Development Group が英国の専門誌 The BMJ に11月20日に発表した。詳細は後記。
これを受けメーカーのGilead Sciences は、remdesivirは米国のNational Institutes of Health and Infectious Diseases Society of Americaや日英独など多くの国家組織から入院患者の標準治療法として認められており、50か国以上で最初の、唯一の承認済み治療法として使用されているのを無視するもので、失望していると述べた。
Remdesivirについて、国際的な臨床試験を行った結果、入院患者の死亡率の改善などには「ほとんど効果が認められないか、全く効果が認められなかったようだ」とする暫定的な結果を発表した。
Remdesivir のメーカーのGilead Sciencesは、WHOのデータは厳格な検証をまだ受けていないもので、これまで別の臨床試験で示された有効性と矛盾しているとする声明を発表した。
2020/10/17 WHO、暫定結果で「Remdesivirの効果認められない」、メーカーは反発
パネルは、ステロイド薬「デキサメタゾン」(Corticosteroids) については推奨するというコメント(強)と推奨しないというコメント(弱)を行なった。
今回の発表を受け、加藤官房長官は、指針について「レムデシビルの効果がないとまでは証明されておらず、また、レムデシビルに効果があるとする十分なエビデンスもないという説明などが記載されている」と述べた。
そのうえで「日本ではアメリカでの緊急使用許可を契機に、複数の臨床試験の結果から一定の有効性が確認できたことから、5月に特例承認を行い、現在、レムデシビルを使った治療がなされている。厚生労働省では特段、承認について見直す必要はないというのが、現時点での認識だと承知している」と述べた。
ーーー
米食品医薬品局は5月1日、Remdesivirを症状の重い入院患者に投与する緊急使用を許可し た。
日本の厚生労働省は海外で先に承認された場合、日本での審査を短縮する「特例承認」を適用し、5月7日、Remdesivirを「特例承認」した。
FDAは10月22日、remdesivirを承認した。Gilead Sciencesは8月にFDAに正式承認の申請をしていた。
2020/10/23 FDA、レムデシビルを正式承認
新型コロナウイルスに罹ったトランプ米大統領は、Remdesivirと、抗体カクテル療法、ステロイド薬「デキサメタゾン」 を使用した。
2020/10/4 トランプ大統領にレムデシビル投与、未承認の抗体カクテル療法も
ーーー
パネルの発表(図)は下記の通り。
https://www.bmj.com/content/370/bmj.m3379
Remdesivirについては下記の各項目でいずれも差がなかったとする。
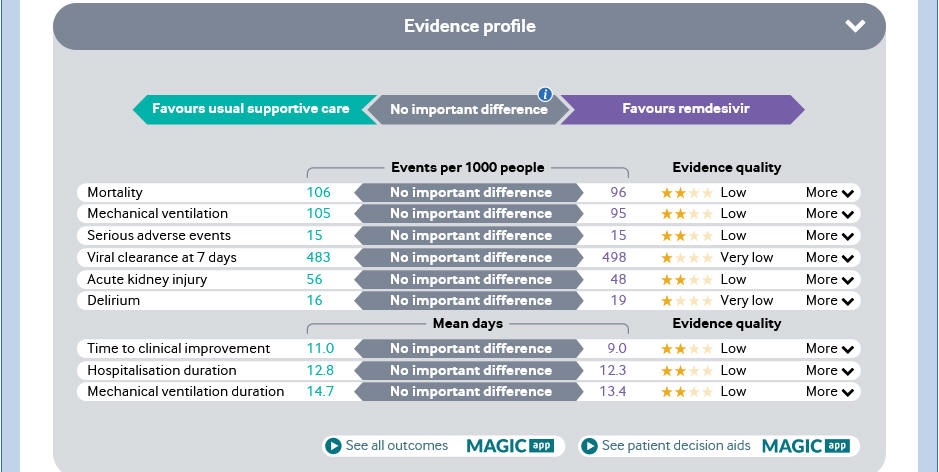
そのほか、手間がかかるとか、コストが高いという点も問題にしている。
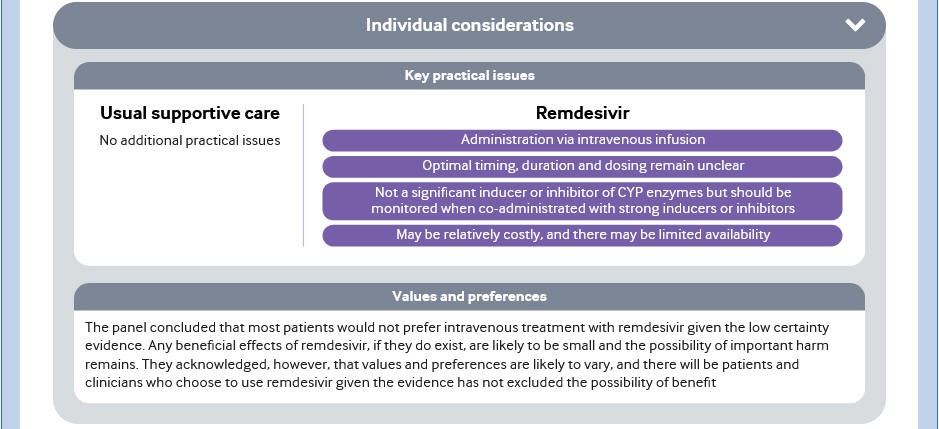
ーーー
ステロイド薬「デキサメタゾン」(Corticosteroids)については、下記の通りで、重症者の死亡率が低いことが利点である。
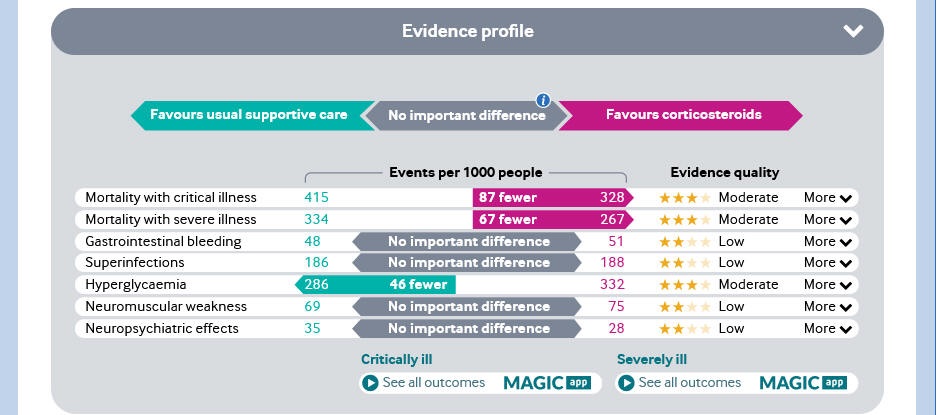
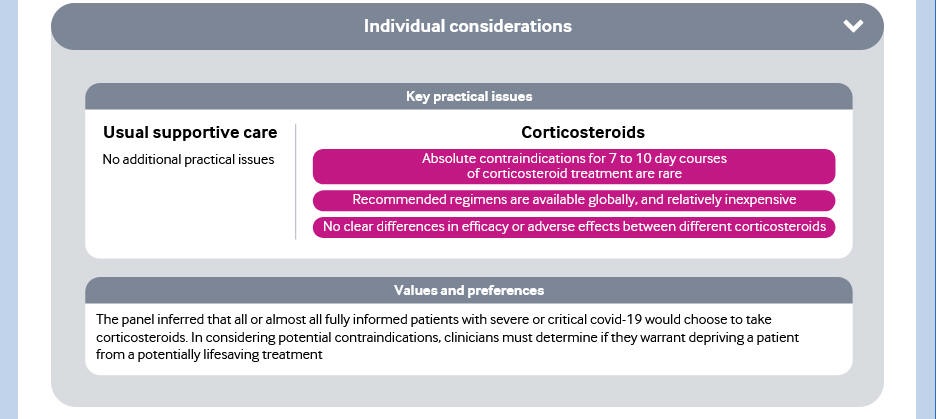
但し、軽症者の死亡率が高いため、推奨しないというコメントもある。

コメントする