厚生労働省の薬食審再生医療等製品・生物由来技術部会は5月24日、第一三共のがん治療用ウイルス「デリタクト注」(一般名:テセルパツレブ:teserpaturev)を条件及び期限付き(7年間)承認とすることで了承された。通常、1か月程度で正式承認される。
付記
6月11日 承認を取得した。
デンカが第一三共からの委託を受けて、五泉事業所(新潟県五泉市)にて本品の生産を担う。
デンカは、がん治療用ウイルス製剤の実用生産を実現するため、2015年に本品の製造工程の開発に着手し、約20億円を投資して五泉事業所にてがん治療用ウイルス製剤の生産に必要な建屋建設と設備導入を進め、2017年10月の竣工を経て、商用製剤生産に必要な製造プロセスの確立により、国内医療機関に必要とされる製剤数の確実な供給が可能になった。
本製品については、7年間に有効性と安全性を評価するためのデータを収集し、改めて承認申請して審査することが求められる。
デリタクトは悪性神経膠腫(原発性脳腫瘍の中でも悪性度の高いグレード3、4)を対象疾患とし、標準治療後の治療選択肢となる。
厚労省によると、この患者数は年間概ね3600例で、同製品の適応患者はさらにしぼられることになる。
東京大学医科学研究所の藤堂具紀教授らにより創製されたもので、第一三共は藤堂教授と共同開発している。
東大側は、非臨床試験から治験製品製造、規制対応、治験実施まで製薬企業が全く関与せずにアカデミアだけで行った日本の医薬品・再生医療等製品開発の歴史に残るアカデミア主導創薬の成功例としている。
培養細胞や動物を用いた安全性や有効性の試験はもとより、臨床試験に用いる治験製品の製造も東京大学医科学研究所内の施設で研究チームが自ら行った。
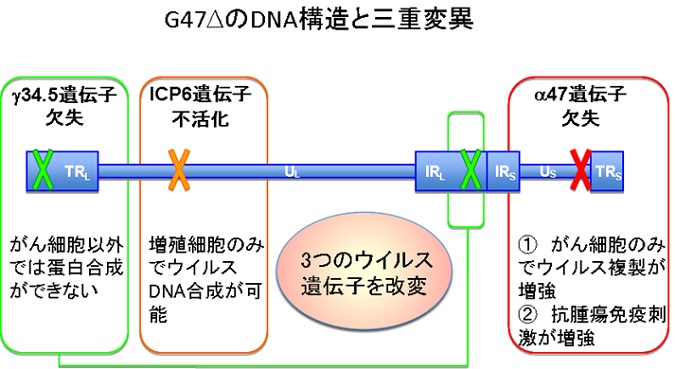
藤堂教授らの研究グループは、単純ヘルペスウイルス1型(口唇ヘルペスのウイルス)に人工的に3つのウイルス遺伝子を改変(三重変異)した第三世代のがん治療用ヘルペスウイルス「G47Δ」の臨床開発を進めてきた。
悪性神経膠腫の一種の膠芽腫の患者を対象に東京大学医科学研究所附属病院で実施した医師主導治験(第II相臨床試験)において、「G47Δ」の高い治療効果と安全性が確認されたため、この治験を主試験として、2020年12月28日に悪性神経膠腫を適応症とする製造販売承認申請が行われた。
G47Δを初めてヒトに投与するいわゆるファースト・イン・ヒューマン(first-in-human)臨床試験は2009年から、膠芽腫を対象とした臨床研究として東京大学で5年間実施され、脳腫瘍内への投与が安全であることが確認された。
更に、有効性を検討する第II相臨床試験は、医師主導治験として、膠芽腫患者を対象に2015年から2020年まで実施し、高い治療効果と安全性を確認した。
G47Δの開発は、発明から実用化まで一貫してアカデミア主導で実施され、日本では新しい治療法開発の様式で成功に至った。厚生労働省の先駆け審査指定制度および悪性神経膠腫を対象とした希少疾病用再生医療等製品の指定を受けている。
今回、「G47∆」(一般名:teserpaturev)」を第一三共が「デリタクト注」の商品名で申請した。
ーーー
神経膠腫(グリオーマ)は原発性脳腫瘍のおよそ4分の1を占める代表的な悪性脳腫瘍である。
神経膠腫は悪性度に従って4段階に分けられ、悪性度の高い2つの段階のもの(悪性度 3と4)を悪性神経膠腫と呼ぶ。
神経膠腫の中で最も頻度が高く、また最も悪性度の高いのが膠芽腫(グリオブラストーマ)で、手術をしてから放射線治療と化学療法を行っても平均余命は診断から18カ月、5年生存率は10%程度で、治癒は極めて困難とされ、全く新しい機序による治療手段の開発が待ち望まれていた。
G47Δは、口唇に水疱ができる口唇ヘルペスの原因ウイルスとして知られている単純ヘルペスウイルス1型の3つのウイルス遺伝子を改変したもの。
単純ヘルペスウイルス1型は、がん治療に有利な特長を多く備えている。
1)ヒトのあらゆる種類の細胞に感染できること、
2)細胞を殺す力が比較的強いこと、
3)抗ウイルス薬が存在するため治療を中断できること、
4)患者がウイルスに対する抗体を持っていても治療効果が弱くならないこと
単純ヘルペスウイルス1型のゲノムから、正常細胞での増殖では必要でがん細胞では不要なウイルス遺伝子を取り除くことで、がん細胞だけで増えるウイルスを造ることができる。
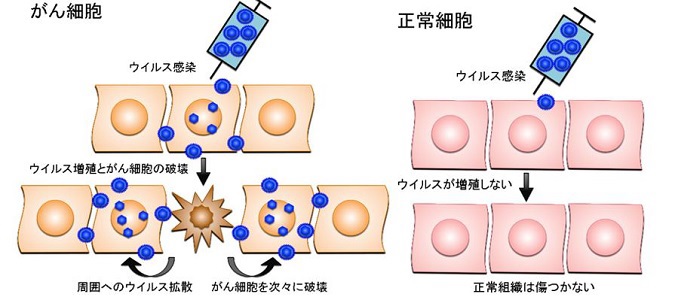
がん細胞だけで増えるウイルスは、がん細胞に感染するとすぐに増殖を開始し、その過程で感染したがん細胞を死滅させる。
増殖したウイルスはさらに周囲に散らばって再びがん細胞に感染し、ウイルス増殖、細胞死、感染を繰り返してがん細胞を次々に破壊していく。
一方、正常細胞に感染した遺伝子組換えウイルスは増殖できないような仕組みを備えているため、正常組織は傷つかない。
既存のがん治療用ウイルスに比べて安全性と治療効果が格段に高くなっている。
また、G47Δの特徴としてがん細胞を破壊する過程で、抗腫瘍免疫を惹起するために、G47Δを投与した部位のみならず、投与していないところにあるがんにも免疫を介して効果が期待でる。
さらに、G47Δは、がんの根治を阻むとされるがん幹細胞をも効率よく破壊することが判っている。
単純ヘルペスウイルス1型を用いたウイルス療法が、悪性脳腫瘍で治療効果を示すことがヒトで確認されて実用化に至ったのは、世界で初めて。
G47Δは脳腫瘍のみならず、あらゆる固形がんに有効であることが動物実験で示されており、今後さらに、可及的速やかに全ての固形がんに適応を広げることを目指している。
2013年からからは、前立腺癌と嗅神経芽細胞腫をそれぞれ対象とした臨床試験を実施した。
2018年からは、悪性胸膜中皮腫の患者の胸腔内にG47Δを投与する臨床試験も開始している。
藤堂教授は、全てのがんに効くと見ており、制度の変更を希望している。(現在は各がんについて臨床試験が必要である。)
コメントする