厚労省の専門部会は8月21日、エーザイと米 Biogenが共同開発したアルツハイマー治療薬「レカネマブ(商品名レケンビ)」について、国内での製造販売承認を了承した。今後、厚労相が正式承認する。正式に承認されれば、認知症の原因物質を除去する初めての治療薬となる。
付記
武見厚生労働相は9月25日、アルツハイマー病治療薬「レカネマブ」を正式に承認した。進行を遅らせる効果を証明した国内初の薬となる。薬価の決定を経て、年内にも医療現場で使えるようになる見込み。
付記
中央社会保険医療協議会は12月13日、「レカネマブ」を保険適用する薬価を承認した。
1瓶200ミリグラムは4万5777円、500ミリグラムは11万4443円で、12月20日から保険適用される。
体重1㌔あたり10ミリグラムを2週間に1回、1時間程かけて点滴する。使用期間は原則1年半となる。体重が50キロの人の場合、年間費用は298万円になる見込み。
実際の患者の負担額は「高額療養費制度」が適用され、数万円程度に抑えられる。
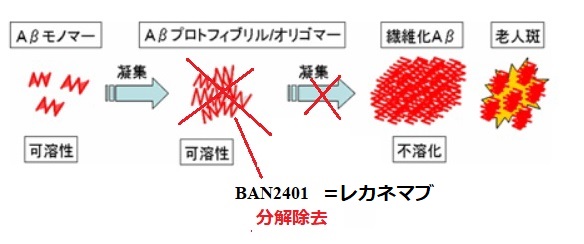
アルツハイマー型認知症は脳内にベータ・アミロイド(Aβ)が凝集し、中間体(Aβプロトフィブリル)が神経変性過程を誘発・促進すると示唆されている。
アルツハイマー病免疫療法には、Aβを投与して生体内でAβに対する免疫反応を惹起させるワクチン療法や、Aβをターゲットとしたモノクローナル抗体を投与する抗体療法がある。
LECANEMABは、アルツハイマー病に対する免疫療法剤創製を目的としたヒト化モノクローナル抗体で、ベータ・アミロイド(Aβ)を分解除去する。
既存の認知症薬は神経の働きを活発にして症状の緩和を図るが、レカネマブは病気の原因となるAβを除去し、進行を抑えることを狙う。
対象は、軽度認知症と、認知症の前段階である軽度認知障害(MCI)の人。壊れた神経細胞の再生は難しいため、症状が進んだ人は対象となっていない。
投与前に脳内にAβがたまっていることを検査で確認。2週間に1回、静脈内に点滴で投与する。
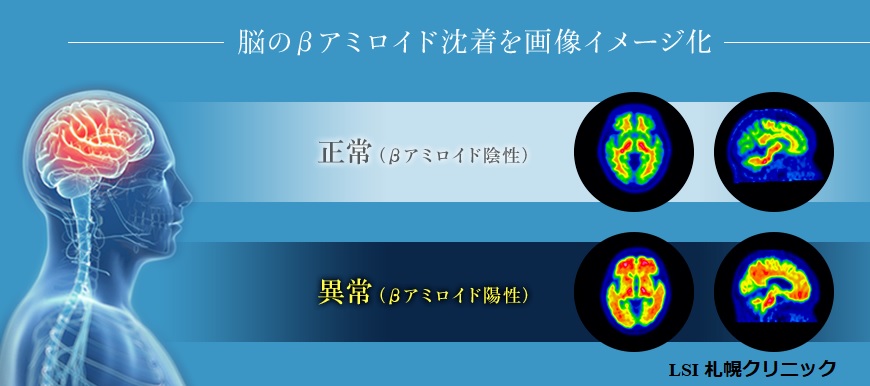
ベータ・アミロイド(Aβ)蓄積の検査方法
(現状) PET検査 (高価)
・体にPET診療用放射性薬剤を注射する。
・投与後約90分で検査薬が異常蛋白と結合する。
・その後、PET装置にて頭部を撮影し、脳内の異常蛋白の蓄積をカラー画像で診断する。
シスメックスは微量の血液からAβの蓄積状態を調べる検査試薬について製造販売承認を取得
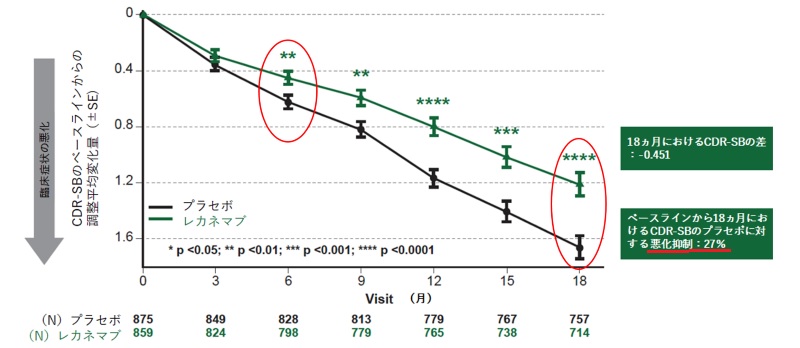
約1800人が参加した国際的な臨床試験(治験)では、18カ月の投与で、偽薬と比べて記憶力や判断力などの程度を評価するスコアの悪化が27%抑えられた。一方で、薬を使った人の12.6%に脳内の浮腫、17.33%に微小出血が報告されるなど副作用も確認された。
エーザイとBiogen, Inc.は2022年11月30日、LECANEMABについて、大規模なグローバル臨床第Ⅲ相Clarity AD検証試験の結果を第15回アルツハイマー病臨床試験会議において発表した。
プラセボとの比較で認知機能の低下を27%抑制したことを報告した。
2022/9/29 エーザイ、アルツハイマー病の新薬で "症状悪化抑える効果確認"
米国では、レカネマブを使う前に、検査で副作用が出やすいとされる遺伝子型かどうかを調べることが推奨された。
この日の部会では、国内では遺伝子検査は求めないが、投与後に脳内の出血を調べることや、血栓を溶かす薬を飲んでいる人への注意喚起を確認した。
8月中に厚労相が承認した場合、実際に日本の医療現場で使えるようになるのは早くて10月、遅くとも11月になる見通し 。
承認後に実際の医療現場で使用するには、 健康保険などの公的医療保険の適用対象とするため薬価を決める必要がある。算定議論は製造販売承認より原則60日から90日ほどかかる。
米国での発売価格 は年間 26,500 ドルで、高齢者向け公的医療保険 Medicare の適用対象になれば、自己負担額は1日あたり14.5ドルになると推定している。
ーーー
エーザイとBiogenは2014年3月に提携を開始した。
現状は次の通りで、アリセプトを除き、開発で提携している。
| エーザイ | アリセプト〈提携対象外〉 (donepezil) |
エーザイの杉本八郎博士らが開発 |
アルツハイマーでは、神経伝達物質のアセチルコリンが脳内で減少している。
アセチルコリンを分解するアセチルコリンエステラーゼの作用を阻害することで、アセチルコリンの濃度を高める。 |
| 新規ヒト化モノクローナル抗体 「BAN2401」LECANEMAB 今回厚労省が承認へ |
2007/12 スウェーデンのBioArctic Neuroscience ABから全世界の研究・開発、製造、販売の独占ライセンスを受ける。 | アルツハイマー病の原因と考えられるベータ・アミロイド成分を除去 | |
| βサイト切断酵素(BACE)阻害剤 elenbecestat「E2609」 x試験中止 |
エーザイが創製
|
アミロイド前駆体タンパク質のβサイト切断酵素であるBACEを阻害することでβアミロイドの総量を低下させる。 | |
| Biogen | 抗アミロイドβ(Aβ)抗体 aducanumab(ADUHELM) |
Neurimmune社より共同開発およびライセンス契約締結のもとに導入 | アミロイド斑(プラーク)は、アミロイドβ蛋白が蓄積したもので、アルツハイマー病患者の脳にみられる。 aducanumab 投与でアミロイドプラークのレベルを下げる |
抗アミロイドβ(Aβ)抗体 aducanumab(ADUHELM)
米国
x→ 申請→FDA優先審査2021/6/7 FDA 迅速承認
2021/6/8 エーザイとバイオジェンのアルツハイマー新薬、米で承認 (迅速承認)→監査部門に調査を要請...........2022/4/11 バイオジェンのアルツハイマー薬、米 Medicareが給付対象を大幅制限
日本
厚労省 継続審議
2021/12/24 エーザイのアルツハイマー新薬、再審議
コメントする