Harvard Medical School のMassachusetts General Hospital は3月21日、遺伝子操作を行ったブタの腎臓を脳死者でない患者に世界で初めて移植したと発表した。同病院では1954年に世界で初めて腎臓移植が行われている。
付記
手術を受けたRick Slayman は5月11日、死亡した。病院側は死因について「移植とは関係ない」としている。
移植を受けたのは重い腎臓病を患っていた男性 Rick Slayman(62)で、手術は3月16日に行われ、4時間に及んだ。術後の経過は順調で、患者は手術から2週間あまりがたった4月3日に退院した。
手術を執刀したのはハーバード大学外科教授の河合達郎医師(67歳)で、2023年8月にMassachusetts General Hospital に新設された臨床移植免疫寛容センター(Legoretta Center for Clinical Transplant Tolerance)の初代所長に就任した。
移植寛容は、臓器移植と同時に骨髄或いは血液幹細胞を移植することにより長期間の免疫抑制剤を必要とせずに、患者の免疫系が新しい臓器を維持することを可能にする革新的な方法で、移植の成功を確保しながら、患者が薬物療法を減らす、又は中止することを可能にする。Legoretta夫妻の2500万ドルの寄付で、移植寛容における世界有数のセンターとなることを目的に設立された。
患者は11年間移植を待ち、2018年に腎臓の提供を受けた。しかし昨年から腎不全の兆候が現れ始め、透析を再開、「末期」との診断が下された。
医師らからブタの腎臓の移植について提案され、男性は「自分が助かるためだけでなく、移植を必要とする多くの人に希望を与えるものだと考えた」と決断に至った経緯を説明した。
河合医師によると(毎日新聞インタビュー)、今回の手術の前にサルで100例以上ブタの腎臓を移植したが、今回、移植直後の腎臓の様子がこれほど良かった例はなかったという。移植した腎臓に血液が流れ始めると 、きれいなピンク色になり、すぐに尿が出た。
人間の場合は腎臓の動脈が2本や3本、たまに4本あることもあるが、ブタはいつも1本で、その意味では実は人間のドナーよりも技術的には簡単だが、今回の患者は透析が難しいほどに血管の病変が進み、移植で使える動脈が限られるなどの難しさはあったという。
今回使用したブタは、米スタートアップの eGenesisが、拒絶反応が起こりにくくなるように遺伝子を改変したもの。ゲノム編集技術「CRISPR/Cas9」が2012に登場し、2015年に同社が創業した。
eGenesisは、ハーバード大学の遺伝学者 George Church と30歳のMs. Luhan Yang(Chief Scientific Officer )が2015年に共同設立した。
人間の病気や臓器の拒否反応の原因となり得る特定の遺伝子を不活性化することで、豚の臓器を人間に移植可能なものにすることを目指している。
この手術で使用されたドナー腎臓(EGEN-2784)は、同社の腎移植のリード候補であり、以下の3つのクラスの編集をした。
(1)ハイパーアキュート(超急性)拒絶に関与する糖鎖抗原の合成に関与する3つの遺伝子のノックアウト、
(2)拒絶を調節する経路の調節に関与する7つのヒトトランスジェンの挿入:炎症、先天性免疫、凝固、および補体、
(3)豚のゲノム内の内因性レトロウイルスの不活化。
遺伝子改変を行わない場合、豚の腎臓は人間の受容体によって直ちに拒絶される。eGenesisは、臓器の安全性と有効性を解決するために、これらのすべての編集を持つ臓器を開発している業界で唯一の企業。
河合医師は5年ほど前まで異種移植をあきらめかけていた。2000年代初め、異種移植後の急性の拒絶反応を抑えるため、Gal(ギャル)という抗原を生む遺伝子をノックアウト(欠失)させたブタが登場したが、その腎臓をサルに移植してもせいぜい100日くらいまでしか生きられず、その先の展望が見えなかった。
そこにクリスパーが登場、さらに多くの拒絶や感染を引き起こす可能性のあるブタの遺伝子を除去したり、特定のヒトの遺伝子を追加したりすることが簡単になった。
それからまた試してみようかという雰囲気になった。
eGenesisと共同研究を始めたのは2017年ごろで、新しいドナーのブタの作製が続けられ、河合医師らは週2~3例のペースでサルでの移植を続けた。免疫抑制法を工夫するなどしてついに術後2年以上生存させることに成功し、これならヒトでも可能かもしれないと思ったという。
過去にゲノム編集されたブタの心臓移植を2人の患者が受けている。
1人目は2022年1月、2人目は23年9月に手術を受けたが、いずれも2カ月足らずで死亡した。
Massachusetts General Hospital の医療チームは、さらに多くの患者でゲノム編集したブタの腎臓移植を実施すべく、正式な臨床試験を開始する予定だが、さしあたり、スレイマンの健康維持に主な焦点を置いている。
ーーー
明治大学発ベンチャーのポル・メド・テック社とeGenesis は、eGenesis が開発した遺伝子改変ブタを日本で再現生産することに成功した。3頭のブタが2024年2月11日に誕生し、今後前臨床研究のために日本国内の医療機関に供給される予定。
ポル・メド・テックは、明治大学バイオリソース研究国際インスティテュートにおける遺伝子改変ブタ作出技術の事業化を目的に2017年2月に設立された。
事業内容は、
医療用ブタによる臓器移植・再生医療事業
疾患モデルブタの製造販売事業
技術サービス事業
2023年9月にポル・メド・テックはeGenesisから遺伝子改変ブタ細胞を輸入し、明治大学バイオリソース研究国際インスティテュートで開発された体細胞核移植技術を用いてクローン子豚を作製した。
実績を有する遺伝子改変ブタのクローン個体が日本で誕生したことにより、今後我が国での臨床応用実現に向けての取り組みが加速化されることが期待される。
ーーー
東京慈恵医科大や国立成育医療研究センターなどの研究チームが、重い腎臓病の胎児にブタの腎臓を一時的に移植する臨床研究を計画している。年内にも、国が認定する委員会への研究計画の申請を目指している。
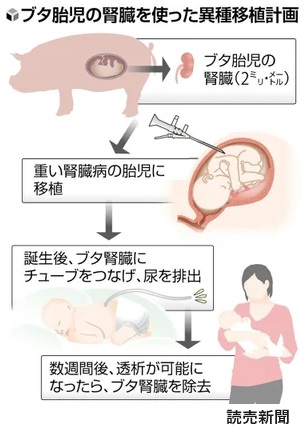
腎臓に問題がある「ポッター症候群」の胎児に、受精後30日のブタ胎児から取り出した約2mmの腎臓を移植する。移植手術は出産予定日の約4週間前に行い、胎児の背中の皮下に特殊な注射針でブタの腎臓を注入する。
ポッター症候群は、生まれつき腎臓が正常に作られず、体内の水分や老廃物を十分に排出できない病気で、5000~1万人に1人の頻度で発症するとの報告もある。妊娠中に羊水の量が少なくなることで見つかり、肺などに障害が出る。生後、透析が受けられないと、間もなく死亡するケースが多い。
移植した腎臓は周囲の血管と自然に結合し、1日数十ml 程度の尿を作ることが期待できるという。出産後、赤ちゃんの背中にチューブを挿入し、たまった尿を排出する。
治療は、赤ちゃんが透析を安全に受けられるようになるまでの数週間、病気の腎臓の代役となる「橋渡し」との位置づけで、その後、ブタの腎臓は取り除くという。
チームの横尾隆・慈恵医大教授(腎臓高血圧内科)は「亡くなるのを見守るしかなかった赤ちゃんの命を救える可能性がある」と話す。
コメントする