血液検査で発症前から診断できるようになれば、早期治療につながる。(PET検査は施設が限られており、費用も高く、早期診断には向かない。)
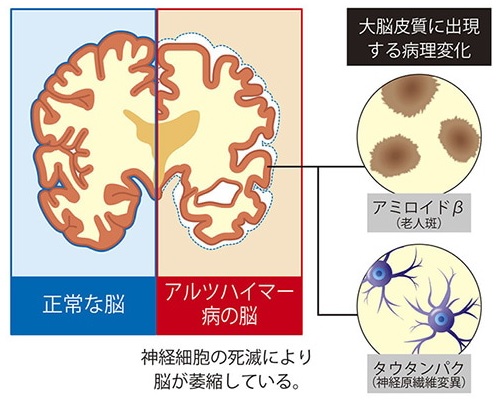
アルツハイマー病では、神経細胞の外側ではアミロイドβ(Aβ)が蓄積して老人班を形成し、神経細胞の中では「タウタンパク」が蓄積してタンパク質が糸くず状に変化したようなもの(神経原繊維変化)が見られるようになる。
2023年9月25日にエーザイのアルツハイマー病治療薬「レカネマブ」が正式に承認された。進行を遅らせる効果を証明した国内初の薬となる。
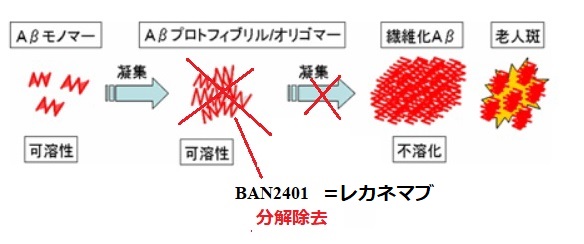
既存の認知症薬は神経の働きを活発にして症状の緩和を図るが、レカネマブは病気の原因となるAβを除去し、進行を抑えることを狙う。
この薬の対象は、軽度認知症と、認知症の前段階である軽度認知障害(MCI)の人で、壊れた神経細胞の再生は難しいため、症状が進んだ人は対象となっていない。
そのため、PET検査で対象かどうかを判断する必要があるが、PET検査の実施できる施設は限られており、費用も高い。他に脳脊髄液検査もあるが、一般的でない。
なお、シスメックスは 微量の血液からAβの蓄積状態を調べる検査試薬について製造販売承認を取得
2023/8/23 厚労省の専門部会、エーザイのアルツハイマー治療薬「レカネマブ」の国内での製造販売承認を了承、近く承認へ
このため、より簡便な評価法への期待が高まっている。
過去30 年にわたり、血液を用いた AD 脳病理変化の推定は困難であったが、近年血液バイオマーカーの開発が加速し、AD 患者の血漿中に検出される Aβ やリン酸化タウなどの病因タンパク質の変化を測定することにより、PET 検査や脳脊髄液検査に匹敵する診断能力が得られる可能性が示されてきた。
しかし認知症期に先行する MCI 期や、さらに早い無症候期(プレクリニカル期)などの超早期段階における性能は十分に実証されておらず、さらに人種差の検討や、日本人における検討も十分に行われていなかった。
プレクリニカル(期)AD : 画像診断やバイオマーカーにより、脳にアミロイドβ蓄積などAD の病理学的変化の存在が推定されるが、認知機能は正常である状態をいう。
プロドローマル(期)=MCI 期AD : ADの病理学的変化があり、客観的にも物忘れなどの認知機能低下症状を認めるが、日常生活機能は保たれており、まだ認知症に至っていないと診断される時期。
研究グループは、Aβ の蓄積が始まっているが無症状であり、発症の前駆時期と考えられる「プレクリニカル期」や、認知機能の低下はあるが認知症に至っていないMCI 期の AD の人を診断・追跡し、予防・治療法の実現を目指す研究を 2019年から開始し、2024 年 4 月末の時点で、700 名の参加者に対してアミロイド PET スキャン、血液バイオマーカー測定等の検査を行ってきた。
今回、474 名の血液検体を対象に、測定結果や臨床データを組み合わせることにより、脳アミロイド検出の標準となる PET 画像の視覚的診断結果をどの程度正確に予測できるかを検討した。
その結果、Aβ と p-tau217(スレオニン 217 リン酸化タウ)血液バイオマーカーを組み合わせることにより、AD の超早期段階における脳 Aβ 蓄積の存在を高い精度で予測できることが分かった。
バイオマーカーで陽性の場合、PET検査で脳アミロイド蓄積がみつかり、陰性の場合は蓄積がなかった。

今後、簡便な臨床的評価と血液バイオマーカーの検査を組み合わせることによって、従来よりも効率的にプレクリニカル期 AD やプロドローマル AD の診断が可能となることを実証し、血液バイオマーカーの実用化と、抗 Aβ薬などを用いた AD の早期の予防・治療のさらなる実用に繋げてゆく。
コメントする