岡山大学学術研究院医歯薬学域 消化器外科学分野の藤原俊義教授らの研究グループは2025年12月15日、食道がんに対して開発を進めてきた腫瘍溶解ウイルス製剤「テロメライシン」を、岡山大学発バイオベンチャーの オンコリスバイオファーマ㈱(英名 Oncolys BioPharma) から厚労省に医薬品製造販売承認申請を行った。
テロメライシン(Telomelysin、OBP-301、Suratadenoturev)は、岡山大学で開発された国産の抗がんウイルス製剤で、感染したがん細胞を殺傷するとともに放射線に対する感受性を増強することが明らかとなっている。
テロメライシンは、風邪ウイルスの一種のアデノウイルス(5型)の E1 領域に、多くのがん細胞で活性が上昇しているテロメラーゼという酵素のプロモーターを遺伝子改変によって組込み、がん細胞中で特異的に増殖してがん細胞を破壊することができるようにしたウイルス製剤。
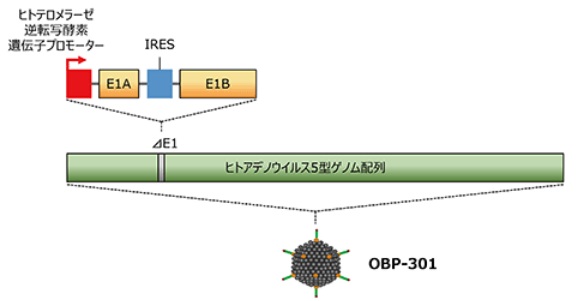
5型のアデノウイルス自体は風邪の症状を引き起こすもので、自然界の空気中にも存在する。テロメライシンは、テロメラーゼ活性の高いがん細胞で特異的に増殖することでがん細胞を溶解させる強い抗腫瘍活性を示す。
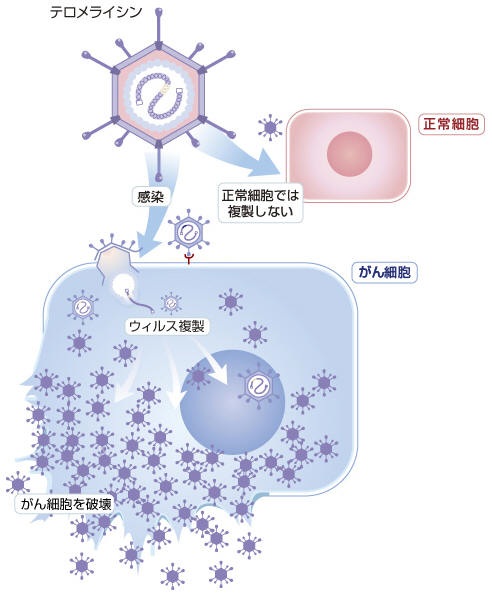
テロメライシンがヒトのがん細胞に感染すると一日で 10 万~100 万倍に増え、がん細胞を破壊する。
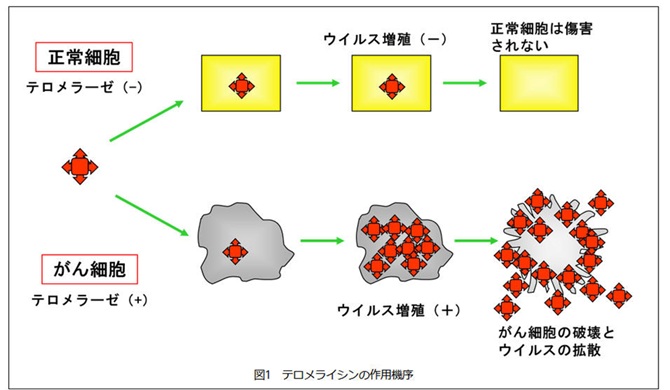
正常な細胞の中ではテロメラーゼ活性が低くテロメライシン®の増殖能力が極めて低いため、臨床的な安全性を保つことが期待されている。
|
|
体の負担も少なく、これまで嘔吐・脱毛・造血器障害などの重篤な副作用は報告されていないことから、患者のQOL(Quality of Life)の向上が期待される。
テロメライシンは、放射線治療や化学療法剤との併用により、更に強力な抗腫瘍活性が導き出せることも明らかになっている。
テロメライシンは放射線によるがん細胞のDNA 損傷の修復を阻害し、放射線治療の感受性を格段に増強することができる。
さらに近年の研究により、ウイルス療法によって破壊されたがん細胞は、その特異的な抗原のシグナルを樹状細胞等の免疫細胞に直接伝えることにより、がん免疫を誘導できることが示唆されており、抗PD-1 抗体等の免疫チェックポイント阻害剤との併用により、全身的な抗がん作用が期待されている。
対象疾患は、食道がん、胃・胃食道接合部がん、肝臓がんなどの固形がんで、今回、食道がん用について承認申請を行ったが、胃がん、肝臓がんについても開発を進めている。
なお、特許については、日本のほか、下記の諸国で取得している。
米国、欧州(14カ国)、南ア、シンガポール、ニュージーランド、オーストラリア、中国、香港、韓国、カナダ。
ーーー
岡山大学で開発されたテロメライシンの臨床試験は、2006 年から米国食品医薬品局(FDA)の承認のもと、米国での安全性を確認する第 I 相臨床試験から始まった。
その後、基礎研究でテロメライシンが放射線治療の効果を強める現象が明らかとなり、2013 年からは岡山大学で外科手術や抗がん剤治療などの標準治療ができない食道がん患者にテロメライシンと放射線治療を併用する臨床研究を実施した。
また 2017 年からは、岡山大学と国立がん研究センター東病院で同様のプロトコールでオンコリスバイオファーマが第 I 相企業治験を行い、2020 年からは岡山大学病院を含む食道がん治療のハイボリュームセンター(全国 17 施設)での多施設共同で第 II 相企業治験が実施さた。
テロメライシンは、2019 年に独立行政法人医薬品医療機器総合機構(PMDA)による迅速審査が受けられる「先駆け審査指定制度」の対象品目に指定されており、今回、PMDA と検討を重ね第 II 相臨床試験での有効性が確認されたことから、2025 年12 月15 日、オンコリスバイオファーマから厚労省に標準治療が難しい食道がんに対する腫瘍溶解ウイルス製剤「テロメライシン」の医薬品製造販売承認申請が行われた。
テロメライシンは、2019 年に医薬品医療機器総合機構(PMDA)による迅速審査が受けられる「先駆け審査指定制度」の対象品目に指定されており、今後、PMDA による審査を受けた後、厚労省の薬事審議会の部会で審議され、原則通り申請後 6 ヶ月ほどで製造販売承認に至ることを見込んでいる。
テロメライシンの販売は、オンコリスバイオファーマと販売提携契約締結を結んでいる富士フイルム富山化学が行う予定。
ーーー
オンコリスバイオファーマは、2004年3月に腫瘍溶解ウイルスの研究開発及び分子標的抗腫瘍薬の研究開発を目的に設立された。東京証券取引所グロース市場に上場している。
ウイルス学に立脚した技術を駆使して、がんや重症感染症の治療法にイノベーションを起こし、世界の医療に貢献することを使命としている。
ウイルスの増殖能力を利用してがんを殺す「がんのウイルス療法」と、ウイルスの増殖を抑制して治療に貢献する「重症ウイルス感染症治療薬」を事業領域とし,ウイルスを軸にした『ウイルス創薬』を展開している。
特にがん領域では、「がんを切らずに治療する」というコンセプトに基づき、がんのウイルス療法テロメライシン(OBP-301)をはじめとする腫瘍溶解ウイルスの開発を行っている。さらに、がんの局所治療のみならず、全身へ転移したがんの治療を可能とするため、免疫チェックポイント阻害剤や他の治療法との併用に関する開発を推進している。
今後は、がんや重症感染症領域に留まらず、オーファンドラッグ(希少疾病用医薬品)領域にも拡大し、難病治療に寄与することを目指す。
OBP-301の上市に伴い同社自身が製薬会社になることで、医薬品の開発トレンドや大手製薬会社の戦略に左右されるライセンス収入に依存したビジネスモデルから脱却し、「継続した医薬品の製品販売収入が得られる製薬会社型事業モデル」と「ライセンス先のイベント達成によりマイルストーン収入などを得るライセンス型事業モデル」のハイブリッドモデルへ変革させていく方針。


最近のコメント