国内の20~55歳の健康な75人を対象に本治療薬服用時の体内動態、安全性、忍容性の確認を行う。初回投与後の安全性上の懸念は確認されて いないという。
付記
同社は国内第2/3相臨床試験を9月27日に開始した。2021年7月より国内第1相臨床試験を開始したが、現時点で、安全性上の大きな問題は認められておらず、薬物動態についても、目標とする血中薬物濃度を上回る良好な結果が確認されている。
新型コロナウイルス(SARS-CoV-2)は3CLプロテアーゼというウイルスの増殖に必須の酵素を有している。
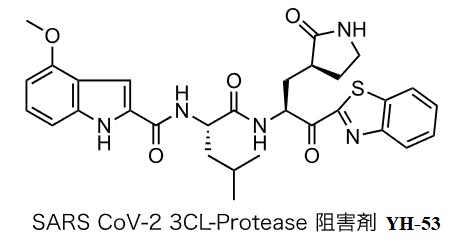
本治療薬は、塩野義が創製した3CLプロテアーゼ阻害薬で、SARS-CoV-2の3CLプロテアーゼを選択的に阻害することで、SARS-CoV-2の増殖を抑制 する。
感染初期に服用することで重症化を防ぎ、発熱やせきなどの症状を改善できると見込む。
SARS-CoV-2感染動物を用いた非臨床試験において、ウイルス量を速やかかつ有意に低下させることが確認されている。
形状はまだ決まっていないが、口から飲む錠剤やカプセルなどを想定している。
ーーー
ウイルスのプロテアーゼ阻害剤は、AIDSやC型肝炎の特効薬として知られている。
- 東京薬科大学は2020年7月31日、群馬大学医学部との共同研究により、2013年に開発した重症急性呼吸器症候群コロナウイルス(SARS-CoV)の3CLプロテアーゼに対する阻害剤 YH-53が新型コロナウイルス(SARS-CoV-2)の増殖を強く抑制することを確認した と発表している。
COVID-19治療薬の候補と考えられ、また、ウイルスの増殖抑制によりCOVID-19の重症化を軽減できる可能性もあるとしている。
- ーーー
国内で承認されている新型コロナの治療薬と、準備中のものは下記の通り。塩野義の3CLプロテアーゼ阻害薬が加わる。
1. レムデシビル:抗ウイルス薬(エボラ出血熱用に開発)
メーカー Gilead Sciences 対象 主に中等症や重症患者 承認 FDA 2020/5/1 EUA 日本 2020/5/7 特例承認 2020/5/1 レムデシビル、5月にも特例承認
2. デキサメタゾン:ステロイド剤(重度の肺炎・リウマチなどの薬)
メーカー (一般の抗炎症剤) 対象 主に中等症や重症患者 承認 英 2020/6/16 標準治療に 日本 2020/7 使用承認 2020/6/17 COVID-19 重症患者にステロイド剤デキサメタゾンが効果
3. バリシチニブ(オルミエント) :関節リウマチなどの薬
メーカー 日本イーライリリー 対象 主に中等症や重症患者 承認 FDA 2020/11/19 レムデシビルとの併用でEUA 日本 2021/4/27 使用承認 2021/4/23 厚労省、3つ目のコロナ治療薬承認
4. カシリビマブ / イムデビマブ:抗体カクテル療法
メーカー Regeneron、Roche / 中外製薬 対象 主に軽症や中等症患者 承認 FDA 2020/11/21 EUA 日本 2021/7/19特例承認 2021/7/21 新型コロナウイルス感染症の抗体カクテル療法を承認
ーーー
・ アクテムラ :抗リウマチ薬
メーカー 中外製薬 Roche/Genentech 承認 FDA 2021/6 EUA 日本 年内申請 2021/6/28 中外製薬の抗リウマチ薬「アクテムラ」、FDAが新型コロナウイルス治療薬として緊急使用許可
・ AT-527:C型肝炎ウイルス治療の経口薬
メーカー Atea Pharmaceuticals Roche / 中外製薬 2021/2/25 中外製薬、Rocheから新型コロナの経口新薬候補導入
・ アビガン :抗インフルエンザウイルス薬
メーカー 富士フィルム 承認 日本 2020/12 継続審議 2020/12/22 厚労省審議会、アビガン承認見送り、継続審議
コメントする