富士フイルムは、iPS細胞を使った移植医療について臨床試験(治験)を国に申請する。
骨髄移植した人の約4割がかかる急性移植片対宿主病(GVHD:graft versus host disease) の患者数十人を対象に2019年に始める。
移植片対宿主病(GVHD)は、移植時に輸注されるドナーの造血幹細胞浮遊液中に含まれるドナー由来のリンパ球が引き起こす合併症で、患者の正常細胞を異物として認識して攻撃する。
皮膚炎や肝炎のほか下痢や嘔吐を繰り返し、命を落とすこともある。
造血幹細胞浮遊液中に含まれるドナー由来のT細胞が活性化され、炎症性サイトカインが放出されることで発症する。患者とドナーのヒト白血球抗原(HLA)の組み合わせの違いに関係する。
おおよそ移植後6-30日頃におこる急性GVHDと、移植後3ヶ月以降に発症する慢性GVHDに分けられる。
今回の治験は、他人のIPS細胞から、過剰な免疫の働きを抑えるとされる間葉系幹細胞(軟骨や脂肪などに変化する細胞)を量産して注射し、移植した骨髄に含まれる免疫細胞が患者の体を攻撃するのを抑え、症状を改善する。
他人の骨髄から採取した間葉系幹細胞を使ったGVHDの治療そのものは実績があり、日本でもJCRファーマが2015年に製品化した。
JCRファーマ(旧称 日本ケミカルリサーチ) は2015年9月に、日本初の他家由来の再生医療等製品として急性移植片対宿主病の治療製品「テムセル®HS注」[一般名: : ヒト(同種)骨髄由来間葉系幹細胞]の製造販売承認を取得し、2016年2月に発売した。
健康な成人から採取した骨髄液からヒト間葉系幹細胞を分離し、培養した。
JCRファーマと医薬品卸のメディパルは、2011年7月より共同で液体窒素を用いた超低温管理物流システムの研究をすすめてきたが、このシステムを稼働させることによって、マイナス150℃以下という極めて低い温度を10日間以上維持した配送・保管が可能となり、緊急時にも、安定した品質の製品を全国の医療現場に届けられる。
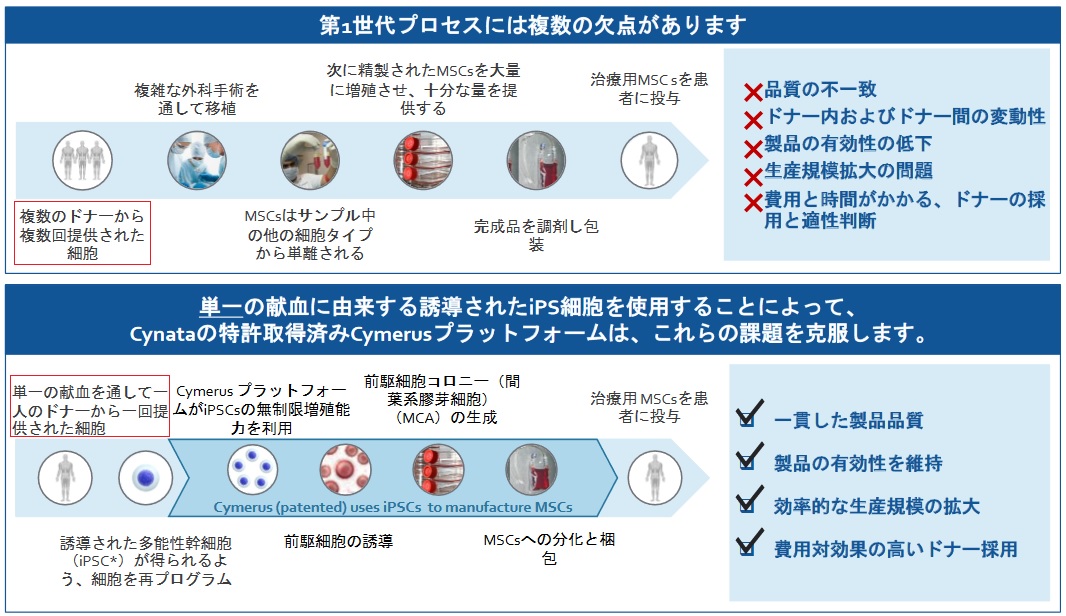
ただ、間葉系幹細胞は増やすことが難しく、多くの提供者を探さなければならない。これには下記の問題があるが、iPS細胞の場合にはそれらの問題がない。
富士フィルムが 出資する豪州のCynata Therapeuticsは、他家iPS細胞由来間葉系幹細胞を用いた再生医療製品を英国で治験中で、15人中14人が完治したり、症状が改善している。
Cynata Therapeuticsは下記の説明をしている。
富士フィルムではCynata Therapeuticsの技術を使って、白血病の治療に伴って重い合併症になった患者を対象として、2022年の製造・販売承認を目指す。
日本で年間1千人以上が重症化し、このうち通常の治療が効かず、今回の臨床試験の対象となるような最重症患者は年間数百人程度発生しているとされる。
ーーー
富士フィルムは2016年9月、2013年設立の豪州のCynata Therapeutics に400万豪ドル(9%)出資することで合意した。
出資により富士フィルムは、Cynata社が移植片対宿主病の患者を対象に臨床試験を予定している他家iPS細胞由来間葉系幹細胞を用いた再生医療製品の開発・製造・販売ライセンス導入と製造受託の選択権を取得した。
(フェーズ 1 試験終了後90日まで)
・ 3百万ドルのマイルストーン投資
・ 富士フイルムはすべての開発と費用に対し責任を持つ
(フェーズ2 以降)
・ 富士フイルムはマイルストーン(60万ドル+)と製品販売に関する2桁台のロイヤルティを支払う。
・ 富士フイルムのGvHD市場予測は年間3億米ドルのピーク収入を示しており、年間3,000万米ドル以上のロイヤルティの可能性
また、Cynata社の持つ、他家iPS細胞由来間葉系幹細胞を用いた再生医療製品開発に関する技術・ノウハウも取得可能となる。
Cynata Therapeuticsは富士フイルムの米子会社Cellular Dynamicsから、iPS 細胞の提供を受けており、この関係で出資が決まった。
Cellular Dynamics については 2015/4/14 京都大学iPS 細胞研究所、Cellular Dynamics Internationalと提携へ
コメントする