Eli Lillyは4 月17日、食事療法および運動療法のみでは血糖管理が不十分な2 型糖尿病の成人患者を対象に、経口GLP-1 受容体作動薬 Orforglipron の安全性と有効性を評価する第 III 相 ACHIEVE-1 試験で肯定的なトップライン結果を発表した。
Orforglipron は、時間を問わず、飲食および飲水の制限なく服用することが可能な初めての飲み薬である。(1 日1 回服用)
Orforglipronは初めての経口低分子 GLP-1 受容体作動薬として第 III相試験で統計学的に有意な有効性を示し、各群の平均 HbA1cを 1.3~1.6%低下させた。
Orforglipronを 1日 1回経口投与し、主な副次評価項目の 1つとして検討した体重減少量は、最高用量群で平均 16.0ポンド(7.3 kg)(7.9%) だった。
ACHIEVE-1における Orforglipron の全般的な安全性と忍容性のプロファイルは、注射剤のGLP-1受容体作動薬と同様であった。
Eli Lillyのミッションは、成人患者数が 2050 年までに 7 億6千万人に達すると予測される2 型糖尿病をはじめとした慢性疾患を減らすことで、今回の結果は、そのミッションに向けた大きな歩みとなる。本剤が承認されれば、供給に制約なく全世界で Orforglipron を上市できる見込みとしている。
2型糖尿病とは:
最も多いタイプの糖尿病で、一般的に"糖尿病"と表現した場合2型糖尿病を示すことが多い。
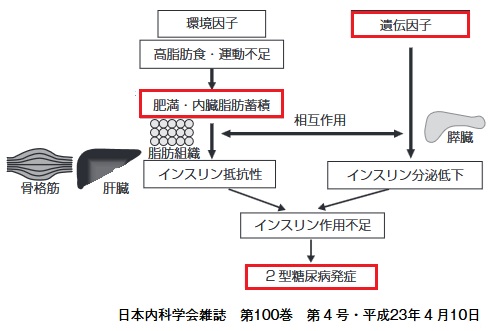
遺伝的素因によるインスリン分泌能の低下に、環境的素因としての生活習慣の悪化に伴うインスリン抵抗性が加わり、インスリンの相対的不足に陥った場合に発症する。一般的に生活習慣病と称されるタイプの糖尿病が2型糖尿病で、インスリン分泌能の低下が不可欠で、生活習慣の乱れだけではなく、大なり小なり糖尿病になりやすい遺伝的素因を持っている。
肥満は、遺伝的な原因に関係なく、2型糖尿病の重大な危険因子となる。
血糖の濃度(血糖値)が何年間も高いままで放置されると、血管が傷つき、将来的に心臓病や、失明、腎不全、足の切断といった、より重い病気につながる。また、著しく高い血糖は、それだけで昏睡などをおこすことがある。
糖分を含む食べ物は消化酵素などでブドウ糖に分解され、小腸から血液中に吸収される。
食事によって血液中のブドウ糖が増えると、すい臓からインスリンが分泌され、その働きによりブドウ糖は筋肉などへ送り込まれ、エネルギーとして利用される。
インスリンの相対的不足に陥った場合に2型糖尿病を発症する。
食事をとると小腸から分泌され、インスリンの分泌を促進する働きをもつホルモンをインクレチンといい、GIP(グルコース依存性インスリン分泌刺激ポリペプチド )とGLP-1(グルカゴン様ペプチド-1)がある。
2型糖尿病に対する治療薬として注目されるのがGLP-1である。
GLP-1は、食事をとって血糖値が上がると、小腸にあるL細胞から分泌され、すい臓のβ 細胞表面にあるGLP-1の鍵穴 (受容体) にくっつき、β 細胞内からインスリンを分泌させる。GLP-1は、血糖値が高い場合にのみインスリンを分泌させる特徴がある。摂取した食物の胃からの排出を遅らせる作用や食欲を抑える作用などもある。
GIPも食欲を抑制するだけでなく、体内での糖分や脂肪の分解を改善する可能性がある。
GLP-1もGIPも肥満症治療薬として使われる。(2型糖尿病治療薬として使われるのはGLP-1)
Orforglipron (OWL833) は中外製薬が初期段階前まで開発した後、2018年に全世界での開発・販売の権利をEli Lillyに譲渡した。
Eli LillyはOWL833に関する全世界の開発権および販売権を取得する。
中外製薬は5,000万米ドルの契約一時金を受け取り、今後の開発の進捗度合いに応じて追加の支払いを受け取る。
また、上市成功後には、中外製薬はさらに売上額に応じたロイヤルティを受け取る。Eli Lillyによると、実用化できれば売上高の1桁台半ばから10%台前半までの段階的なロイヤルティーを中外製薬に支払う。仮に6兆円の売り上げで12%の料率なら、約7000億円が中外製薬に入る計算である。
中外製薬にとって、糖尿病・肥満症領域は主力分野ではない。そのため、Eli Lillyにライセンスした。
同社がこれをタイミング良く開発できたのは、同社の開発体制にある。まず創薬技術を開発してそれを医薬品開発に適用する「技術ドリブン創薬」を掲げる。他社のようにターゲットとする疾患領域を定めてから開発に取り組むのと発想が異なる。
研究開発に集中できるのは、スイスの親会社ロシュとの役割分担がうまくいっているためである。
ーーー
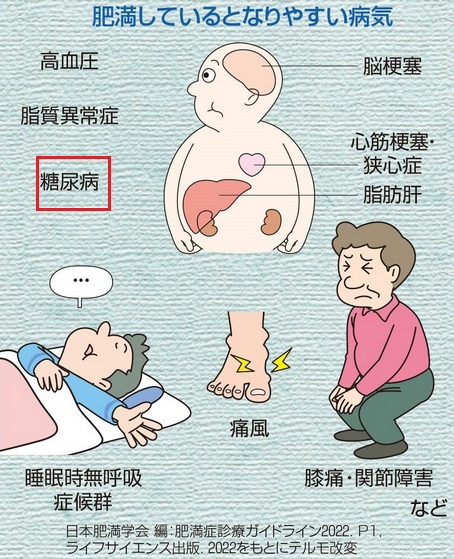
肥満は2型糖尿病の重大な危険因子となるが、他にもいろいろな病気の原因となる。
新タイプの肥満症治療薬の利用者が、米国を中心に世界で急増している。GLP-1、GIP を使うものである。
先駆けとなったのが、デンマーク製薬大手Novo Nordisk のWegovy(ウゴービ )で、2021年に米国で承認された。もともと糖尿病(内臓脂肪の蓄積が主な原因)のために開発した薬(GLP-1受容体作動薬)を肥満症治療に応用したもので、食欲を抑制することでやせる効果があるとされる。日本では「セマグルチド(遺伝子組換え)」として2023年3月に承認された。
米Eli Lillyは2023年12月、同様の働きを持つ肥満症治療薬Zepboundを米市場に投入した。
CNBCによると、各社の開発状況は下記の通り。これまでの治療薬はすべて注射である。
|
製品名 |
メーカー | 用法 | 米承認 | |
| Wegovy | Novo Nordisk | 週1回の注射 | 2021 承認 | GLP-1を活性化 |
| Zepbound | Eli Lilly | 週1回の注射 | 2023 承認 | GLP-1とGIPを活性化 |
| Saxenda | Novo Nordisk | 週1回の注射 | 2020 承認 | GLP-1を活性化 |
| MariTide | Amgen | 月1回の注射 | Experimental | GLP-1を活性化し、GIPをブロック |
| Danuglipron | Pfizer | 1日1回の錠剤 | Experimental | GLP-1を活性化 |
| VK2735 | Viking Therapeutics | 週1回の注射 | Experimental | GLP-1とGIPを活性化 |
| Pemvidutide | Altimmune | 週1回の注射 | Experimental | GLP-1を活性化 |
| GSBR-1290 | Structure Therapeutics | 週1回の錠剤 | Experimental | GLP-1を活性化 |
| Survodutide | Zealand Pharma, Boehringer Ingelheim |
週1回の注射 | Experimental | GLP-1とグルカゴンを活性化 |
2024/4/15 新タイプの肥満症治療薬が急増。
参考
京都大学病院はiPS細胞から作った膵臓の細胞のシートを糖尿病の患者に移植する臨床試験を2025年にも実施する。
2024年9月3日 京大、iPSで糖尿病を治療
| お願い
システムミスで古いデータについては、①画像が出ない、②他のデータ(http://www.knak.jp/) に飛べない、という問題が出ました。 恐れ入りますが、過去のデータについてはバックナンバー (目次つき) でご覧ねがいます。 |
...

コメントする