|
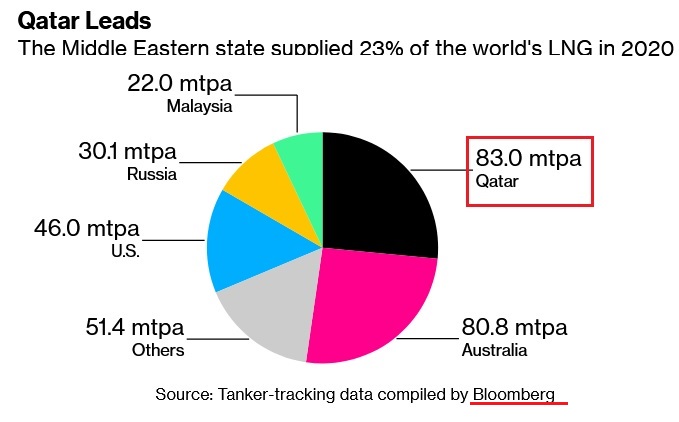
Qatar PetroleumのNorth Field East Project が順調に進んでいる。 カタール政府は2017年7月、液化天然ガス(LNG)の大増産計画を発表した。凍結していたNorthfield の南部の新しいガス田を開発する。 Qatar Petroleumは2021年2月8日、North Field East Project の最終投資計画を決定したと発表した。 世界最大のLNG計画で、QatarのLNG生産能力を年産77百万トンから110百万トンに引き上げる。
Northfieldガス田から新たに生産される日量約60 億立方フィートの天然ガスを液化処理する。 LNGに加え、コンデンセート、LPG、硫黄、ヘリウムも生産する。2025年第4四半期にスタートする予定。 建設費総額は 287.5 億米ドルに達する。 環境対策として、温室効果ガスを既存 LNG プラント比 25%以上削減する二酸化炭素回収・貯留設備 がある。 同日、千代田化工とフランスのTechnipEnergiesが本計画のLNG輸出基地(新規液化天然ガスプラント)に関する設計、調達、建設及び試運転業務を受注した。 North Field East Project はLNG拡張計画の第一弾であり、第二弾のNorth Field South ProjectではLNG能力を110百万トンから126百万トンに拡大する。更なる拡大も検討中。 Qatar Petroleum は2021年3月30日、 Qatargas Liquefied Natural Gas Company 1のJV契約を契約期限の12月31日で 終了し、2022年1月1日以降、Qatar Petroleumの100%子会社にすると発表した。
Qatar PetroleumはNorth Field East Project を従来の海外勢とのJVではなく、単独で実施するとみられ、既存のJVについても契約期限が来ると順次、契約を終了すると見られる。 Qatar Petroleum はNorth Field East Project 推進にあたり、社債の発行を決めた。同社は7月1日に125億米ドルの社債を発行した。
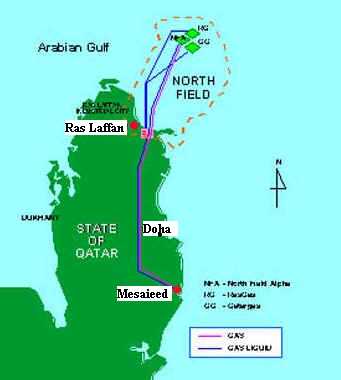
ーーー 2010年にカタールでLNGの増産工事が完了、国家目標としてきた年産7700万トン体制が完成した。 Qatargas 1は1998年に完成したが、その後、次々に完成、2010年2月のRasGas の第7系列780万トンに続き、同年中にQatargasの第6、第7系列、各780万トンが完成した。 世界最大級のNorth Fieldガス田から産出する天然ガスをRas Laffanで液化する。
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
「no」と一致するもの
Wall Street Journalは8月25日、米半導体大手Western Digitalが、同業のキオクシアホールディングス(旧東芝メモリホールディングス)を買収する交渉が大きく進展していると報じた。
買収額は200億ドル(約2兆2000億円)規模で、早ければ9月中旬にも合意する可能性があるとしている。
ただ、キオクシアが株式上場を選択したり、別の企業に買収されたりする可能性も残っているとしている。
Wall Street Journalは、2021年3月にも、Micron TechnologyとWestern Digitalがそれぞれ個別にキオクシア買収を検討していると報じた。
キオクシアは昨年、上場を図った。
東証は2020年8月27日、上場を承認した。同社は10月6日上場を予定し、時価総額は2兆円を超えるとみられた。
しかし、直前に大口取引先である中国の華為技術(Huawei)に対する米政府の取引規制で 収益性の急激な低下が予想され、先行きへの不透明感が高まったため、上場を延期し、上場の時期を慎重に検討することとした。
2020/8/31 キオクシア、10月に上場
キオクシアは再申請を目指しており、8月27日の取締役会で東京証券取引所への上場申請を諮る予定だったが、見送った。
同社は、上場案のほかに、他の選択肢、Western Digitalとの合併も視野にいれていると見られる。Western Digital との協議がこの数週間で加速したと報じられている。
付記
「WDとの合併について、経済産業省からは容認論が出ている」との報道があるが、中国が合併を承認しないだろうとの見方が強い。
一方、「中国企業はWestern Digitalやキオクシアのメモリチップを必要としており、中国政府がノーということはない」との見方もある。
ーーー
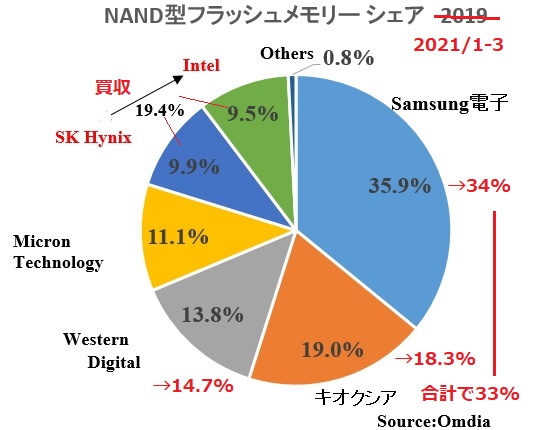
キオクシアとWestern Digital は日本でNAND型フラッシュメモリーの生産を共同で行っている。
NAND型フラッシュメモリーの世界のシェアは下図の通り。今年1~3月の トレンドフォースのデータでは、両社を合わせると、トップのSamsung電子に肉薄する。
ーーー
キオクシアとWestern Digital は日本でNAND型フラッシュメモリーの生産を共同で行っている。
発端は1999年の東芝と米国のSanDiskとのNAND型フラッシュメモリ事業に関する提携の基本合意である。
2000年5月にNAND型フラッシュメモリの製造合弁会社の設立
社名:FlashVision LLC
立地:バージニア州(東芝子会社Dominion Semiconductor内に700億円の設備投資)
出資比率、製品引取比率:50/502002年4月に「フラッシュビジョン(旧:Flash Vision LLC)」を東芝四日市工場内に移転
以降、順次増設、両社の出資比率はたびたび変更
詳細は 2017/4/14 東芝の半導体売却に新たな難問
Western Digial はハードディスクドライブ(HDD) 専業メーカーで、2011年に日立から事業を買収して大きくなった。
Western Digital は2015年10月21日、SunDisk を190億ドルで買収すると発表、2016年5月12日、買収手続きを完了した。
2017/5/5 Western Digital の歴史
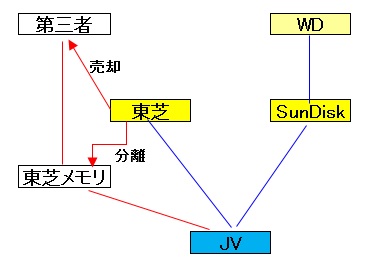
経営再建中の東芝は2017年4月に半導体のメモリー事業を分社化し、買収を前提に新会社「東芝メモリ」を発足させた。SunDiskとのJV持ち分も移管した。
これに対し、Western Digitalがクレームを付けた。
2017/5/15 東芝の半導体事業売却、Western Digital が差し止め申し立て
以降、下記の推移:最終的に東芝メモリとWestern Digital は和解し、このあとも共同で日本での生産を行っている。
2017/7/17 東芝とWestern Digital の法廷闘争
2017/8/8 東芝、東芝メモリの増設を単独実施
2017/9/7 東芝メモリの売却、9月13日に決定(岩手県北上市に新規拠点)
2017/9/22 東芝、東芝メモリの「日米韓連合」への売却発表
2017/12/14 東芝、Western Digital と和解
東芝メモリとWestern Digital は、係属中の仲裁および訴訟を解決し、フラッシュメモリ事業に関する協業を一層強化することで合意した。
建設中の最先端メモリ製造棟である四日市工場第6製造棟への今後の設備投資について共同で実施する。両社は2019年5月、北上市に東芝メモリが建設中の北上工場第1製造棟において両社共同で設備投資を実施する正式契約を締結した。
2018/9/21 東芝メモリ 四日市工場 第6製造棟およびメモリ開発センターの竣工
2019/7/19 東芝メモリ、「キオクシア㈱」に改称
2020/10/29 キオクシア、四日市工場で新製造棟 を建設
キオクシアの当初の出資者は下記の通りで、SK Hynix は将来の事業参加を狙っている(契約上、いろいろな制限を付けられている)が、他の海外株主は上場を通じて高値での売却を狙っている。
東芝も元々は売却を狙ったが、それまでの事業運営上、40%の出資を続けている。
SK Hynix を除く各株主は、売却価格次第では、売却に賛成すると思われる。
(単位:億円)
| 出資 | 議決権 | 転換社債 | 議決権なし | |||
| 東芝 | 3,505 | 40.2% | 1,096 | 2,409 | ||
| HOYA | 270 | 9.9% | 270 | 0 | ||
| (日本側計) | (3,775) | (50.1%) | ||||
| Bain | 2,120 | 49.9% | 1,361 | 759 | ||
| SK Hynix | 3,950 | 15% | 1,290 | 2,660 | ||
| (Bain/SK) | (6,070) | |||||
| Apple | 4,155 | 4,155 | ||||
| Seagate | ||||||
| Kingston Technology | ||||||
| Dell Technologies Capital | ||||||
| 合計 | 14,000 | 2,727 | 1,290 | 9,983 | ||
両社は、生産は共同で行っているが、販売は完全に別の法人としてやっており、統合には各国の独禁当局の承認が必要である。
General Motors は8月20日、火災が相次いだ電気自動車「Chevrolet Bolt EV」について、バッテリーの製造上の欠陥による火災の危険性を理由に、事実上全面リコールを決定した。
GMはBolt EVで火災が数回発生したことを受け、昨年11月、バッテリーの最大充電量を90%に制限するソフトウェアアップデートを行った。
しかし、アップデート後も火災が発生したため、バッテリーモジュールを交換することにし 、本年7月23日にリコールを届け出、2017-19年の生産分(約6万9千台 、うち米国で5万1千台)についてバッテリーモジュールの部品を交換するリコールを実施してきた。
最近のGMによる調査では、2019年以降の生産分でも製造上の欠陥が見つかった。陽極タブの破れやセパレーターが曲がる可能性があると述べた。充電中に発火につながる危険性がある。
今回、リコール対象を直近の生産分まで拡大し、2019年以降に生産され、販売されたBolt EVと派生モデルのBolt EUV 7万3千台に対する追加リコールを発表した。これでGMが生産したすべてのBolt EV がリコールの対象になる。
2019年モデルの残り 9,335台(うち米加 8,201台)
2020-2022モデル 63,683台(うち米加 61,422台)
新たにリコール対象となった車両には充電率を90%に制限するアップデートを行い、その後の精密診断を通じ、欠陥が発生したバッテリーモジュールを交換する。交換するバッテリーモジュールには8年間/10万マイル(16万km)の保証をつける。
GMは「Bolt EVの所有者は、火災リスクと被害を防ぐため、リコール前までは最大充電量を90%に制限し、 従来より頻繁に充電し(残り運転距離を70マイル以下にはしない)、充電後、直ちに屋外に駐車すること」と伝えた。
ーーー
Bolt EVはLG Energy Solutionが生産したバッテリーセルをLG電子がモジュール化したバッテリーを搭載している。
LG Energy Solutionは、忠清北道清州市の梧倉工場と米ミシガン州Holland工場 (LG子会社Compact Power)でバッテリーセルを生産し 、複数のバッテリーセルをまとめてモジュール化し、GMに納入して いる。
LG Chemは2020年12月1日に電池部門を分社化し、LG Energy Solutionを設立した。
2020/9/19 LG Chem、電池部門を分社化
本年10月にIPOを予定していたが、最近、上場予備審査終了期限が延期された。本件が影響している可能性がある。
ーーー
GMとLG Chemは2020年5月に折半出資でUltium Cells LLCを設立、オハイオ州Lordstown の近辺に23億ドルを投資してEV用バッテリー工場を建設している。Ultium Cells LLCは2021年4月16日、テネシー州 Spring Hillに約23億ドルを投資し、新型電池Ultiumバッテリーの工場を建設すると発表した。Lordstown 工場に次ぐ米国で2カ所目のEVバッテリー生産工場となる。
2020/1/3 GMとLG Chem、世界最大級のEV用電池工場建設計画を発表 付記
ロイター通信は、GMがLGからリコール費用の賠償に関する約束を取り付ける方針だと報じた。
GMが今年7月にバッテリーモジュールの交換を決めた際には、リコール費用を8億ドルと想定し、LG電子が約2億ドル、LG Energy Solutionが0.8億ドルのリコール引当金を4-6月期の業績に反映させた。
今回、GMはリコールに10億ドルを投じる。合計18億ドルになる。
LGは「顧客企業と共にリコール措置が円滑に取られるよう積極的に協力していく。原因調査の結果が出れば、費用負担率と引当金の額が決まる」と説明した。
EV業界関係者は「現在は完成車メーカーがバッテリーメーカーの責任を追及した場合、たとえ不服でも賠償責任を逃れるのは難しい。バッテリーの完成度を高めることがカギになる」と語った。
LG Energy Solution は10月12日、リコール費用の負担額でGMと合意したと発表した。
リコール費用は全体で2兆ウォン程度と見られるが、LG側が1兆4千億ウォン(約1300億円)を支払う。
今回のリコールは、LG Energy Solution製のバッテリーを搭載したフォルクスワーゲンAG ID.3 EV で火災が発生して1週間後から始まった。
事故は8月14日にオランダのフローニンゲンで発生した。充電を終えた状態で運転手は後輪の方から出ている煙を確認した。運転手と子どもはすぐに車から出て人命被害はなかったが、車両は全焼した。
ーーー
現代自動車とLG化学は3月4日、火災が相次いだ電気自動車(EV)のリコール費用の負担比率を巡って最終合意した。世界で計8万1700台のリコール費用約1000億円のうち、電池を供給したLG化学が約7割、車両メーカーの現代自が約3割を負担する。
対象車種は現代自が韓国や米国、欧州で販売したEV「Kona Electric」と「IONIQ」など。電池システムをすべて交換する。
LG Energy Solutionは当初、同社が提案した急速充電のロジックが現代のバッテリー管理システムで誤って利用されたと主張し、バッテリーセルを出火リスクの直接的な原因とみなすべきではないと表明した。しかし、係争が長引けばブランドイメージの低下につながると判断し、早期の幕引きを図った。
現代自は「顧客の不便と市場混乱を最小化すべきだとの意見でLG化学と一致した」とコメント。LG化学側も「消費者安全を最優先とし、リコールに積極的に協力する」と語った。
米下院は8月24日、3兆5000億ドルの予算決議案を可決した。
ーーー
バイデン大統領は3月31日、国内のインフラの整備等に8年間で2兆2500億ドルを投入する新たな計画 American Jobs Plan を発表した。
2021/4/2 バイデン大統領、American Jobs Plan 発表、8年間で2兆2500億ドル投資
この計画は最終的に2つに分けられた。
米上院は8月10日、5500億ドル規模のインフラ包括法案を賛成69、反対30で可決した。
共和党 民主党 民主系
無所属合計 賛成 19 48 2 69 反対 30 30 棄権 1 1 合計 50 48 2 100
政府と民主党は、これから除外された教育や子育て支援、気候変動対応などの10年間で3.5兆ドルの予算を予算決議案の形で提案した。
予算の内容と、財源として増税を含んでいることから共和党の賛成は見込めず、過半数の賛成で通せる予算決議案の形をとった。
上院は8月10日、3兆5000億ドル規模の予算決議を50対49の賛成多数(民主党のみの賛成)で可決した。
共和党 民主党 民主系
無所属合計 賛成 0 48 2 50 反対 49 49 棄権 1 1 2021/8/11 米上院、5500億ドル規模のインフラ包括法案を可決、下院採決時期は不透明
これを受け、下院は夏期休会中であったが、開会した。
政権と民主党のペロシ下院議長は3兆5000億ドル規模の予算決議を先に通すことを決めた。
予算決議案は上院で可決されたが、この後、各委員会がこれに基づき財政調整法案を策定し、予算委員会でまとめられ、一つの包括的な法案として議会で審議され、両院で可決することが必要である。
インフラ包括法案を棚上げし、上院での3兆5000億ドル規模の予算成立の担保にしようというもの。
しかし、民主党内の進歩派の9人(その後1人が加わる)が自らが優先課題として掲げる項目を多く盛り込んだインフラ包括法案をさきに可決することを求めた。双方の折り合いがつかず、24日未明に採決を見送った。
その後、ペロシ議長が、超党派のインフラ投資法案を9月27日までに採決すると約束し、下院はインフラ法案などの審議を進める手続き上の採決と一体にして予算決議をようやく可決した。
共和党 民主党 合計 欠員 賛成 220 220 反対 212 212 棄権 合計 212 220 432 3
予算決議では、決議に基づき具体的な税制・支出法案を策定する委員会の期限を9月15日に設定している。非常に厳しい日程である。
その後、財政調整法案は上下両院で採決が行われる。財政調整措置では、共和党のフィリバスター(議事妨害)はないため、民主党は上院での賛成多数(50対50だが、同数の場合は上院議長である副大統領が投票する)で可決することが想定されている。
但し、民主党内にも増税や 財政膨張を懸念する議員は多い。上院では民主党議員全員の賛成が必要だが、インフラ投資法案を9月27日までに採決してしまうと、増税などへの慎重論を抑える手立てはなくなる。このため、内容の修正を迫られる可能性もある。
ーーー
下院は同日、共和党優位の州における投票権制限に向けた動きに対抗するために民主党議員が提案した法案を賛成多数で可決した。ただ、上院では10人の賛成が必要だが、現在支持を表明している共和党議員は1人だけであり、可決する見込みは薄い。
共和党 民主党 合計 欠員 賛成 219 219 反対 212 212 棄権 1 1 合計 212 220 432 3
法案は1965年に制定された人種差別を禁じる「投票権法」の主要な保護規定の効力を復活させる内容。
投票権法では、各州などの投票に関する規則変更を阻止する権限が盛り込まれていたが、2013年の最高裁判断で無効とされた。この権限を司法省に改めて与えるのが法案の柱である。
投票権法の第4条では、「投票に関する法律を変更する際に、連邦政府または連邦裁判所の承認を得なければならない」としていた。差別が顕著だった9州や郡などを指定して、選挙の実施方法の決定などの管轄権を連邦政府に移管、選挙に関する手続きを変える際は事前に連邦政府の許可を得ることを義務づけ、差別の復活を阻止していた。
米連邦最高裁判所は2013年6月25日、この投票権法第4条を無効とした。
差別が顕著だった9州や郡などを指定して いるが、同条項は当初5年の期限だった。しかし、連邦議会が繰り返し延長、投票権法が成立した1965年から50年近くが経過した現在、南部の「状況は劇的に変わった」と述べ 、無効とした。
状況が大きく変わっているのに、50年前に問題であった特定地域の扱いを継続するのは問題であるとするもの。
今回の法案は投票に関する規則変更を阻止する権限を司法省に改めて与えるのが柱。
今年に入り少なくとも18州が投票権を制限する州法を制定した。 期日前投票の期間を制限し、郵便投票で提出が必要な本人確認書類を増やし、各党による投票所監視要員の権限を強化するなどで、不正対策に必要との議論がある一方で、民主党側は人種的少数派が投票するのを困難にする狙いで成立させていると批判してきた。
共和党上院トップのマコネル院内総務は、投票に関するルールは州レベルの決定に委ねるべきだと述べている。
台湾の蔡英文総統は8月23日、台北市の病院で同日から始まった台湾のワクチンメーカー高端疫苗生物製剤股份有限公司(Medigen Vaccine Biologics Corp) が開発した新型コロナウイルスワクチンの接種を受けた。
台湾では、ModernとAstraZenecaのワクチンの接種が行われているが、総統はMedigenワクチンの完成を待ち、これまで接種を受けていなかった。
ーーー
台湾のワクチンメーカー高端疫苗生物製剤(Medigen)は 、新型コロナウイルスワクチン「MVC-COV1901」を開発している。
組み換えタンパクワクチンで、米国立衛生研究所と共同で開発した。
抗原は、米国立衛生研究所からライセンス供与されている組換えスパイクタンパク質(S-2P)で、抗原をより安定させるために、三量体の融合前の形態を維持することができる。
Dynavax Technologies によって開発された水酸化アルミニウムとCpG1018のアジュバントを使用する。
Medigenは6月10日、開発中の新型コロナウイルスワクチン候補について、第2相の臨床試験の中間解析の結果を公表し た。台湾内の11の病院が協力し、4000 人余りが被験者として参加した。「二重盲検法」で実施し、第三者機関が分析を行った。
ワクチンの中和抗体が、台湾で最も多く接種されている英 AstraZeneca製ワクチンの中和抗体に劣らないというデータが示され、いずれの被験者にも深刻な副反応は見られなかったという。
同社はその後、解析報告などを衛生福利部(保健省)食品薬物管理署に提出し、第Ⅲ相を省略した状態で、緊急使用許可(EUA) を申請した。
20歳以上の成人を接種対象とする。2回の接種を、28日の間隔をあけて接種する 。2~8℃で保管する。
緊急使用許可(EUA)を受けてワクチンを生産する期間中、安全性を示すモニタリング報告書を毎月提出しなければならない。また、承認後1年以内に国内外の接種事例をもとにワクチンの有効性を示すレポートを作成し、提出する必要がある。
Medigenは今年下半期にパラグアイで 第Ⅲ相臨床試験を進めた後、世界保健機関(WHO)の承認を受ける方針。
ーーー
Medigenのワクチンは、第Ⅲ相臨床試験無しで緊急使用許可を得ており、十分時間をかけずに承認されたとの批判が出ている。
最大野党国民党は、台湾の人々の命や健康がワクチンの実験台となるべきでないとして、ワクチン接種に反対している。
同党の元幹部はワクチンの承認を撤回するよう訴訟を起こしたが、先週、裁判所が訴えを退けた。
今回、このワクチン接種を受けたのは蔡総統が初めて 。台湾は海外からのワクチン調達に苦戦しており、自身が接種することで、「国産ワクチン」の有効性と安全性をアピールし、接種率向上を図りたい考え。
Bayerは8月16日、同社の子会社Monsantoのグリホサート系除草剤「ラウンドアップ」が原因でがんになったと訴えた顧客への損害賠償を支持した米控訴裁判決を不服として、米最高裁に上訴した。
付記
Bayerが最高裁に上訴したのは下記のEdwin Hardeman訴訟である。
米最高裁は本件を審査する可能性が出てきた。最高裁は12月13日、政権に対し、最高裁が本件を取り上げるべきかどうかについての意見を求めた。
本件は連邦法 を無視した州法に基づく判決であり、政権は当然、取り上げるべきだと返事すると思われる。
バイエルは先週、ラウンドアップの利用者にそれぞれ数千万ドルの賠償を命じた判決に対する控訴審で敗訴した。
同社は、ラウンドアップががんの原因になったとの訴えについて、健全な科学的知見や連邦規制当局の製品認可に反すると繰り返し主張してきた。
今回の訴訟は、これに加え、連邦法と州法のどちらが優先かということが問題となっている。
訴えはラウンドアップによる発癌である。
(連邦法)米国で農薬承認を行うEPAは発癌性はないとしている。このため、ラベル(使用法等を記載)には「発癌性の危険」の表示はなく、仮に表示すれば違法となる。(FIFRA=Federal Insecticide, Fungicide, and Rodenticide Act )
(州法)しかし、カリフォルニア州はラウンドアップを発癌性製品のリストに含めており、その場合、「発癌性の危険」が表示されていないのは違法となる。
原告側弁護士は、連邦法ではなく、州法を基に訴訟を起こした。
陪審員は、除草剤Roundupのラベルには発癌の危険が示されていないため違法であるとして有罪とし、一審の裁判官も 、控訴裁の裁判官もこれを認めた。
「発癌性の危険」を表示してはいけない連邦法と、表示しないといけない州法のどちらをとるかであり、Bayerは「当然、連邦法が優先」として上告した。
常識的には、連邦法が優先すると思われるが、最高裁の判断が待たれる。最高裁の判断により、Bayerの今後の法廷闘争策が違ってくる。最高裁が受け付けた場合、Bayerはその結果を待ち、当面は和解交渉を行なわないと見られる。却下した場合、和解交渉を進めると見られる。
Bayerは今回、最高裁で不利な判決が出た場合に備え、45億ドルの追加引当金を計上し、和解金や訴訟費用として引き当て済みの116億ドルに上積みした。
ーーー
Bayerは2016年9月14日、Monsantoの買収で合意したと発表した。
米国は2018年5月29日、条件付きで承認した。これで全ての条件が整い、6月7日に買収が完了、MonsantoはBayerの100%子会社になった。買収額は総額625億ドル。
2018/3/23 EU、バイエルのモンサント買収を承認
直後の8月10日に、カリフォルニアの陪審員がモンサントの除草剤 Roundup による発癌被害で289百万ドルの賠償評決を下した。Roundup については、全米で7月末で約8千件の訴訟があるが、最初の裁判である。
その後、多くの裁判が行われているが、今回Bayerが最高裁に上訴したのはEdwin Hardeman訴訟である。
原告Edwin Hardemanは1980年から2012年にかけ、カリフォルニア州北部Sonoma郡の自宅でラウンドアップを定期的に使用。その後、がんの一種である非ホジキンリンパ腫と診断された。
米カリフォルニア州地方裁判所の陪審は2019年3月19日、「Roundup」ががんを発生させた「事実上の要因」だったとの評決を下し、また、「除草剤Roundupのラベルには発癌の危険が示されておらず欠陥である」として、3月27日、被害に対して527万ドル、懲罰的賠償で75百万ドルとした。
サンフランシスコの地裁判事は7月16日、「除草剤Roundupのラベルには発癌の危険が示されておらず欠陥である」との陪審員の判断については否定せず、有罪にした。
被害に対しては527万ドルを認めたが、裁判官は懲罰的賠償は高すぎるとして20百万ドルに大幅に減額した。被害に対して15倍もというのは憲法から認められないとした。
| 原告 | 陪審員 | 裁判官判断 | |
| Edwin Hardeman | カリフォルニア 2019/3/27 | 地裁 2019/7/16 | |
| 損害賠償 | 527万ドル | 527万ドル | |
| 懲罰的損害賠償 | 75百万ドル | 20百万ドル 被害に対して15倍もというのは違憲 |
上記の損害賠償についてMonsantoが新しい裁判を求めたが、裁判官は、拒否した。
2019年12月13日にBayerは本件で「重大なエラー」があり、裁判をすべきでなかったと主張し、上告した。
問題は、「除草剤Roundupのラベルには発癌の危険が示されておらず欠陥である」との陪審員の判断である。
米EPAと司法省は2019年12月20日、Friend of the court brief (=amicus curiae:個別事件の法律問題で第三者が裁判所に提出する情報または意見)を提出した。
このなかでEPAは、EPAはRoundupのラベルを調べ承認したこと、Roundupには発癌性はなく、このため、発癌性の危険を表示する必要性はないとした。判決は覆すべきであるとしている。
EPAは発癌性を認めず、製品ラベルには当然、発癌性の危険は表示されていない。しかし、カリフォルニア州は発癌性製品のリストに含めており、発癌性の危険が表示されていないのは違法となる。
原告側弁護士は、連邦法ではなく、州法を基に訴訟を起こし、一審の裁判官もこれを認めたもの。州法に基づき、連邦法でのラベルを否定した形となっている。
EPAと司法省は、ラベルは法律で認めたもので、それと異なるやり方での使用は法律違反であるとし、州は農薬の販売や使用を制限することは出来るが、国が承認したラベルと異なるもの、追加したものを求めることは出来ないとしている。
2019/12/26 米EPAと司法省、除草剤Roundupの発癌被害裁判でBayer側支持の意見書
控訴裁の合衆国第9巡回区控訴裁判所は2021年5月14日、サンフランシスコ地裁の判断を認めた。
これを受け、Bayerは最高裁に上告した。
ポイント:
原告は、州法に基づき、除草剤Roundupのラベルには発癌の危険が示されておらず欠陥であるとする。
しかし、EPAは繰り返し、発癌危険の警告は不要とし、連邦法のFIFRA(連邦殺虫剤殺菌剤殺鼠剤法)ではEPAの承認なしに警告をつけることは出来ないとする。
連邦法と州法はどちらが優先するか?
世界的な「脱炭素化」の流れをにらみ、本業である鉱業に経営資源を集中させる。 化石燃料から脱却し、「未来に目を向けた」商品へのシフトを目指す。石油、天然ガス部門を巡っては、一部の株主から売却を求める声が強まっていた。
ーーー
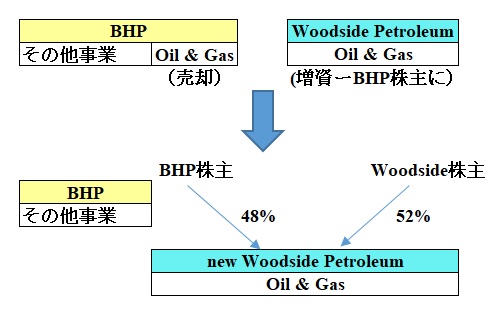
石油・ガス事業の時価総額は185億豪ドル(約1兆5千億円)とされる。
Woodsideは石油・ガス事業の取得と引き換えに新株を発行し、BHP株主に割り当てる。新しいWoodsideの株主は、既存のWoodside 株主が52%、BHP株主が48%となる。
Oil & Gas事業売却後のBHPはロンドン証券取引所への上場を廃止し、オーストラリア証券取引所に一本化する。
BHPはこれまでに、石油ガス事業の売却を進めていた。
Woodside Petroleumは2016年9月5日、BHP Billiton から豪州西部沖のScarborough ガス田などの権益の半分を4億ドルで取得すると発表した。
BHP Billiton がExxonMobil と共有しているガス田の25%分と、BHP Billiton が単独所有するガス田の50%を取得するもので、後者についてはOperator になる。BHP は2018年7月26日、米国のEagle Ford、Haynesville、Permian 及びFayetteville の陸上石油・ガス資産全てを合計108億ドルで売却する契約を締結した。
2018/7/31 BHP、米国の陸上石油・ガス資産全てを売却
BHPの2020年5月期の売り上げ構成は下記の通り(日経)。
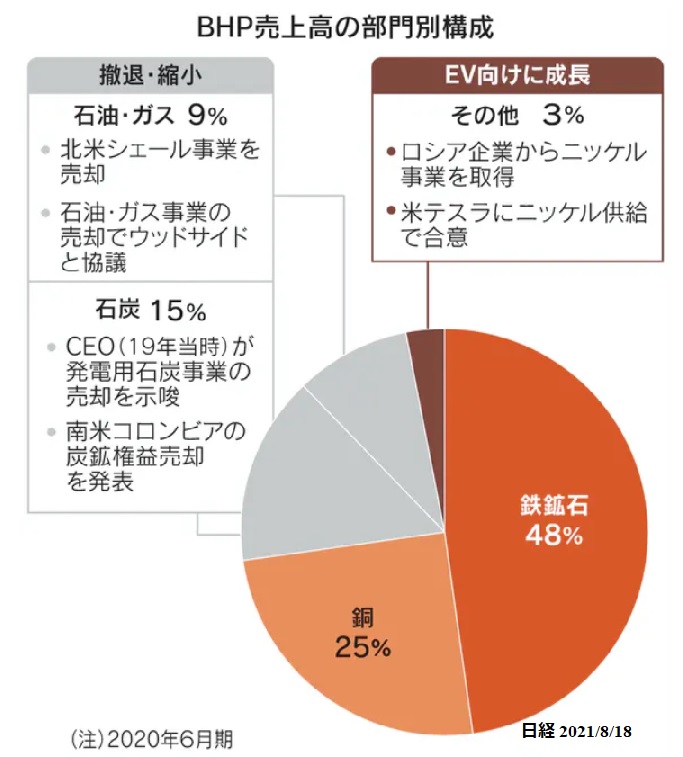
石油・ガス事業から撤退する一方、ニッケル事業を強化している。
BHPは7月22日、EV世界首位の米Teslaにニッケルを供給することで合意したと発表した。
BHPは西オーストラリア州のNickel West ProjectからTeslaに供給を行う。同プロジェクトは、ニッケル地金より利益率が高いとされる硫酸ニッケルの生産を7─9月期に開始する。
両社はまた、ブロックチェーン(分散型台帳)を用いた原材料のトレース(追跡)や、エネルギー貯蔵のソリューションについても検討する。
同社は長年にわたり西オーストラリア州でNickel West事業を行なっているが、一時は売却も目指した。
しかし2019年5月22日に、今後の電気自動車電池の需要に対応するため、硫酸ニッケル事業を拡大する意向を明らかにした。BHPのビーベン最高財務責任者(CFO)は戦略ブリーフィングで、探査か買収の形でニッケル事業の成長を図る可能性があると述べた。Nickel West事業も保有し続けると発表した。
BHPは2020年6月19日、ロシア資源大手Norilsk Nickelから西オーストラリア州にあるニッケル鉱山を取得することで合意したと発表した。
Norilsk Nickel子会社のMPI Nickel Pty Ltd,から下記を取得する。
・Honeymoon Well Nickel Project
・Albion Downs North and Jericho exploration JVの50%(残り50%はBHP Nickel Westが所有→100%に)
直後の6月27日には、BHPはカナダでニッケル探査を手がけるNoront Resourcesに総額3億2500万カナダドル(約280億円)での買収を提案した。
BHP LonsdaleはNoront Resourcesの3.7%を保有するが、全株を取得するTOBを行なうことで合意した。
ーーー
BHPは8月17日、カナダサスカチュワン州のカリウム肥料プロジェクト Jansen Stage 1への57億ドル(約6230億円)投資を承認した。
当初、カナダのカリウム肥料会社の買収に失敗した事が契機で、独自の鉱山開発に乗り出した。鉄鉱石、銅、石炭、石油に続き「第5の柱」になるとし、既に10年間で42億ドルが鉱山と製造設備に投資されたが、未だ操業計画の最初の出荷予定など詳細が公表されておらず、先行きが懸念されていた。
今回の発表では、 年間435万トンを生産する。増産も検討する。建設(地下鉱山、加工工場、倉庫、自動運転の貨車積み込み設備、港湾設備への投資を含む)に約6年かかり、2027年に出荷を予定する。
WHOは2020年3月に、COVID-19の治療のため各国の研究機関を結集してWHO Solidarity Trial Consortiumをつくり、抗ウイルス薬候補4剤(レムデシビル、ヒドロキシクロロキン、ロピナビル、インターフェロンβ-1a)がCOVID-19入院患者の死亡率を減らすことができるかを調べた。
結果はいずれも、入院患者の死亡率を減らすことではほとんど効果がなかった。
今回、Solidarity調査の次の段階としてSolidarity PLUSを開始するが、独立した専門家委員会によって選ばれた既存薬剤3剤の効果を確かめる。
臨床試験は52ヵ国600超の病院から数千人規模の入院患者を登録し、実施される見通し。
選ばれたのは次の3剤:
1) アルネスネート(artesunate)
アルテスネイトは、マラリアの治療に使用される医薬品で、ヨモギ属の薬草Artemisia annua から抽出されるartemisinin誘導体。
インドの多国籍製薬会社Ipca Laboratories が生産する。30年以上、マラリア治療に使われており、極めて安全。
抗炎機能を評価する。
2)イマチニブ(imatinib)
イマチニブは小分子チロシンキナーゼ阻害剤であり、特定の種類の癌の治療に使用される経口化学療法薬で、Novartisが生産する。
初期の臨床データで、肺毛細血管漏出を逆転させることを示唆している。オランダで実施された臨床試験で、安全性の問題がない場合、イマチニブが入院中のCOVID-19患者に臨床的利益をもたらす可能性があることを報告した。
3)インフリキシマブ(infliximab)
ヒトTNFαを認識するキメラモノクローナル抗体であるTNFα阻害剤で、クローン病など免疫システムの病気に使われる。
Johnson and Johnsonが生産。
特定の自己免疫性炎症状態の治療に20年以上承認されており、COVID-19に対して最も臨床的に脆弱な高齢者を含む、広域スペクトルの炎症を制限する上で好ましい有効性と安全性を示す。
WHOのテドロス事務局長は「より効果的でアクセスしやすい治療法を見つけることが依然として切実に必要だ」と強調した。
WHOは既にデキサメタゾンなどのステロイド系抗炎症薬について、致死率を下げる効果があるとして重症者への投与を推奨している。
デキサメタゾン:ステロイド剤(重度の肺炎・リウマチなどの薬)
メーカー (一般の抗炎症剤) 対象 主に中等症や重症患者 承認 英 2020/6/16 標準治療に 日本 2020/7 使用承認 2020/6/17 COVID-19 重症患者にステロイド剤デキサメタゾンが効果
WHOは本年7月、コロナ治療薬のガイドラインを更新し、中外製薬が創製した抗体医薬「アクテムラ」、米Regeneron Pharmaceuticalsの「サリルマブ」を推奨薬剤に追加した。
いずれも炎症を引き起こすIL-6の活性を抑制することで関節の炎症を改善する。
アクテムラ :抗リウマチ薬
メーカー 中外製薬 Roche/Genentech 承認 FDA 2021/6 EUA 日本 年内申請 2021/6/28 中外製薬の抗リウマチ薬「アクテムラ」、FDAが新型コロナウイルス治療薬として緊急使用許可
アルツハイマー型認知症の原因は未だ解明されていないが、進行に伴っていくつかの特有の病変が見られる。例えば、神経細胞の外側では「アミロイドβ」が蓄積して老人班を形成し、神経細胞の中では「タウタンパク」が蓄積してタンパク質が糸くず状に変化したようなもの(神経原繊維変化)が見られるようになる。
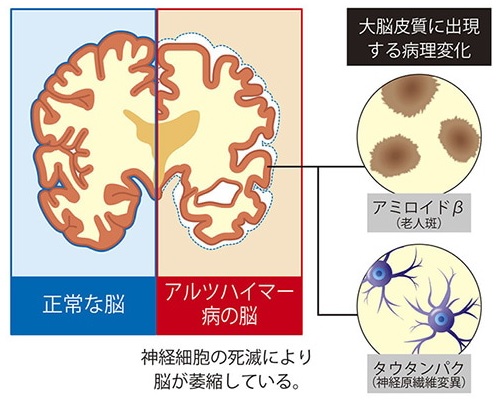
2021/6/25 島津製作所、少量の採血でアルツハイマー病の原因候補物質を測定
1.現在のアルツハイマー治療薬
アルツハイマーは、病理学的には神経原線維変化とアミロイドβ沈着の2つを特徴とする変化により、脳の神経細胞死が生じ、記憶力低下をはじめとする認知機能障害が緩徐に進行する病気。
現時点で認可されているアルツハイマー病の治療薬は以下の4つで、いずれも根治を目的としたものではなく、進行を少し(半年〜1年程度)遅らせるものでしかない。
いずれも、ニューロン間の情報を伝達する化学物質である神経伝達物質を制御することにより機能する。
①アリセプト®(ドネペジル)
②レミニール®(ガランタミン)
③リバスタッチ®、イクセロン®(リバスチグミン)
いずれも、アセチルコリンエステラーゼ阻害薬で、脳内で記憶保持や集中、覚醒などの作用がある神経伝達物質のアセチルコリンの分解を抑制し、脳内の相対的濃度を高めることで、アルツハイマー型認知症やレビー小体型認知症の中核症状の進行を抑制する。
軽度~中等度の段階を中心に幅広く服用されている。
④メマリー®(メマンチン) NMDA受容体拮抗剤
グルタミン酸は脳内の興奮性の神経伝達物質で、この作用を弱めることで、過剰な興奮による脳神経の損傷を抑え、中核症状の進行を抑制する。
比較的重度の認知症にも用いられる。
NMDA受容体拮抗剤とアセチルコリンエステラーゼ阻害剤とは効果をもたらすしくみが異なるため、これらが併用されることもあ る。
2.新薬開発(アミロイドβ仮説)
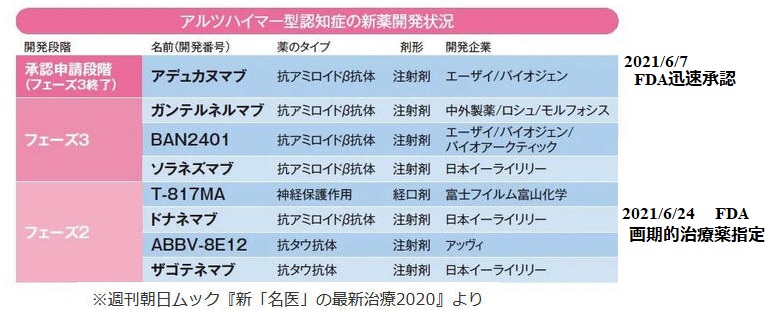
注) 一般名の末尾の「マブ」はモノクローナル抗体医薬の意味。
末尾の「ビル」は抗ウイルス薬、「ニブ」は キナーゼ阻害薬
「Aβ(アミロイドβ)仮説」
脳の神経細胞外にAβが蓄積→タウ蛋白のリン酸化→神経原線維変化→細胞毒性が生じ、神経細胞が死滅→認知症を発症
抗Aβ抗体:Aβを除去
抗タウ抗体:タウを除去したり、タウの凝集を阻害
T-817MA:神経細胞保護効果や神経突起伸展促進効果のあるT-817MA投与で、リン酸化タウの減少を確認。
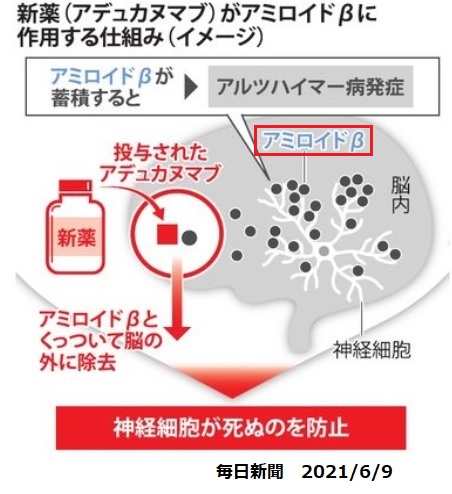
①エーザイ/バイオジェン ADUHELM(一般名:アデュカヌマブ)
米食品医薬品局(FDA)は2021年6月7日、エーザイと米バイオジェンが共同で開発するアルツハイマー型認知症治療薬候補ADUHELM(一般名:アデュカヌマブ)について、脳内のアミロイドβプラークを減少させることにより、アルツハイマー病の病理に作用する初めてかつ唯一の治療薬として、迅速承認(accelerated approval)したと発表した。従来の認知症薬とは異なり、認知機能の低下を長期的に抑制する機能を持つとして世界で初めて承認された。
アミロイド斑(プラーク)は、アミロイドβ蛋白が蓄積したもので、アルツハイマー病患者の脳にみられる。新薬はこのレベルを下げるもの。
2021/6/8 エーザイとバイオジェンのアルツハイマー新薬、米で承認
ADHUHELMについては、2020年11月7日のFDAの末梢・中枢神経系薬物諮問委員会で、有効性に対して否定的な見解が出された。
賛成 反対 保留 アルツハイマー病治療としての有効性に関する説得力のあるエビデンスを示しているか 1 8 2 試験がアデュカヌマブの有効性の裏付けとなるエビデンスを示しているか 0 7 4 アデュカヌマブの薬力学的効果に関して説得力のあるエビデンスを示しているか 5 0 6 302試験をアデュカヌマブのアルツハイマー病に対する有効性に関する主要なエビデンスとみなすことができるか 0 10 1
FDA諮問委員会の提言は、FDAによる審査において考慮されるが、拘束力はない。しかし、提言に反する承認は異例。2019/10/24 Biogenとエーザイ、一旦治験中止したアルツハイマー薬の承認申請へ今回の承認をめぐり、委員会のメンバーのうち、反対票を投じた大学の神経学者と、当日の採決に加わらなかった医療機関に勤める人物の2人が辞任した。委員会の反対にもかかわらずFDAが、条件付きで承認したことへの抗議だという。
このため、FDAのウッドコック長官代行は、承認に至るまでのバイオジェンとFDAとのやりとりが適正だったか調査するよう、米厚生省の監査部門に調査を要求、監査部門は8月4日、承認過程を調査すると表明した。
米下院の二つの委員会も、同薬の承認をめぐる調査に着手した。一方、二つの米大手医療機関は、当面は患者に使用しない方針を表明した。
② Ely Lilly 「ドナネマブ」
Ely Lilly は2021年6月24日、同社がアルツハイマー病に対して開発中の抗体医薬品であるdonanemabがFDAから画期的治療薬指定(Breakthrough Therapy designation)を受けたと発表した。
画期的治療薬指定は、重篤な疾患の治療を目的として、FDAの承認を受けている既存の医薬品と比較して、当該医薬品が臨床的に意義のある評価項目を大幅に改善する可能性が臨床的エビデンスにより示された場合、その開発と審査の迅速化を図ることを目的としている。
今年後半に迅速承認制度に則り donanemabの生物学的製剤承認申請書(BLA)を提出する予定
Aβペプチドは脳内に沈着し、過剰になると互いに結合してタンパク質プラークを形成する。
ドナネマブは、このタンパク質プラークを標的とし、脳内で負担となる余分なタンパク質を除去する。
(単に新しいプラークの沈着または既存のプラークの成長を防ぐのではなく、沈着したプラーク自体を標的にすることが、脳から既存のアミロイド負荷を取り除くために必要)以前のプラーク結合抗体のいくつかは、脳に微小出血を引き起こしたために放棄されたが、これは微小出血を引き起こすことなくマウスのプラークを除去することが報告されている。
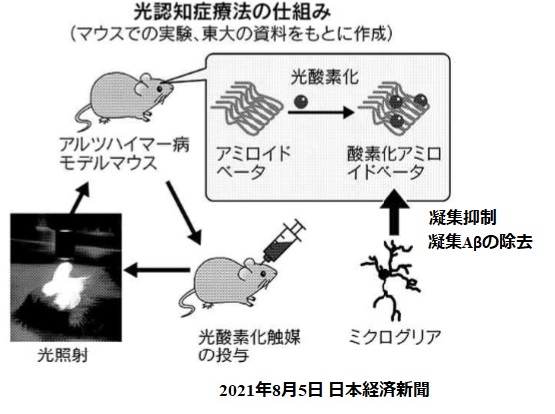
3.光認知症療法
東京大学は2021年4月、光酸素化法を開発したと発表した。
脳内でアミロイドβペプチド(Aβ)が凝集・蓄積することがAD発症の原因と示唆されており、Aβの凝集を抑制すること 、また凝集したAβを効率よく除去することがAD根本治療戦略として考えられている。
今回、光照射と光酸素化触媒を用いた光酸素化法を確立した。
・ 凝集Aβ除去には脳内免疫担当細胞であるミクログリアが関与していることを確認。
・ 光照射と、光によってアミロイド選択的な酸素化活性をもつ低分子化合物である光酸素化触媒を用い、
アミロイドに対して酸素を付加する。
・ 光酸素化された凝集Aβは凝集がほぐれた状態になり、ミクログリア細胞内のリソソーム分解酵素による分解が亢進する。
・ 患者脳内に蓄積したAβに対しても光酸素化が可能である。
凝集Aβに対する光酸素化が、さらなる凝集抑制効果と凝集Aβの除去という2つの効果を有し、AD根本治療戦略となりうる可能性を示した。
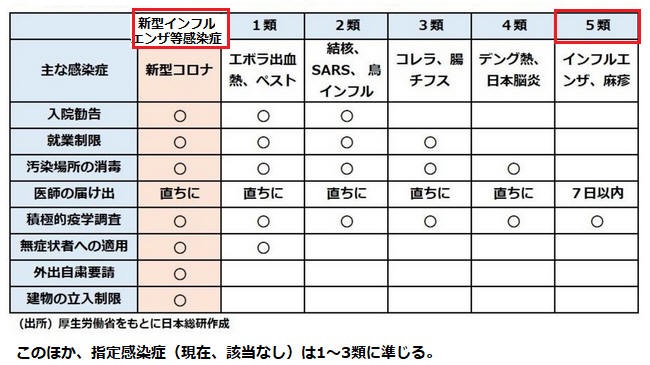
新型コロナウイルスの扱いを、現在の感染法上の「新型インフルエンザ等感染症(2類相当以上)」からインフルエンザと同じ「5類」に引き下げる案が厚労省で議論されていると報じられている。
「新型インフルエンザ等感染症」の場合、無症状者も含めた入院勧告や外出自粛の要請、都道府県による経過報告、感染経路の調査などの措置が講じられる。
感染が疑われると判断された場合には、新型コロナウイルス感染症の検査を受け、陽性と判断されると、一般の医院の手を離れ、保健所が取り扱う。
疫学調査を行い、濃厚接触者を調査し、重症化リスクの高い患者に限定して入院先を決め、軽症者等は宿泊療養・自宅療養で対応する。感染者が増えるにつれ、保健所の機能は麻痺しつつある。入院先が限定されるため、重症者でも入院先がみつからず、自宅療養者が重症化し、死亡する例も出てきた。
コロナ以外の患者の治療に支障が出てきつつある。新型コロナが季節性インフルエンザ並みに軽症だというわけではなく、現在の体制をこれ以上は続けられないという考えである。
これに対し、反対論が沸き起こっている。
しかし、新型コロナを「2類相当以上」にしたのがそもそも問題であり、直ちに「5類」に引き下げるべきだとする医師の発言が注目を浴びている。
尼崎市の長尾クリニックの長尾和弘医師で、
1) インフルエンザ並みの5類に変更せよ、
2) 治療薬イベルメクチンを「スガノメクチン(菅のメクチン)」「スガルメクチン(メクチンに縋る)」として
国民全員に配布せよ
と主張する。
毎日新聞の医療プレミア特集が8月9日付で長尾医師のインタビュー記事「新型コロナ 自宅療養で命を失わないために必要なこと」を掲載した。
8月10日のBSフジ プライムニュース「逼迫する医療現場 大学・医師会・開業医 医療制度の課題を検証 」に出演し、自説を述べた。
他に、大学からは田中雄二郎・東京医科歯科大学学長、医師会からは尾崎治夫・東京都医師会会長が出演した。8月12日の読売テレビ系「情報ライブ ミヤネ屋」にリモート出演した。
ーーー
感染法分類
新型コロナは感染症法分類で「新型インフルエンザ等感染症」に指定され、2類感染症以上の強い対策をとる。
具体的には、外出自粛の要請や入院勧告、指定医療機関への入院などで、無症状者についてもこうした措置を適用することができる。全て保健所が管理するが、患者が増えれば、保健所の業務も増えて対応は遅くなる。実際には入院できず、自宅待機が急増している。
保健師は医師ではないため、重症化リスクの判断はできない。このため、入院調整までの間に亡くなる例が出ている。
ーーー
長尾医師の主張:
尼崎市の長尾クリニックは、外来診療(内科、消化器内科、循環器内科、整形外科、もの忘れ外来、乳腺外来、禁煙外来)と在宅医療(訪問診療、往診、訪問介護、リハビリ、ケアマネジャー)を扱い、年中無休(日曜・祝日の午後のみ休診)で診療している。
昨年4月から約450人のコロナ患者を診断し、約200人のコロナ患者の在宅療養に関わってきた。全員に24時間いつでも連絡を取れるよう携帯番号を教え、必要なら往診をしたり、訪問看護師に点滴などを依頼したりした。
初診時に血中酸素濃度が60%という重症呼吸不全の患者が2人いて、1週間後に入院できたが、自宅療養中は大量のステロイド剤を投与する治療法など懸命の治療に取り組み、2人とも救命できた。入院できずにすべて自宅で治療し回復した人も約100人いる。
在宅管理をした約200人のコロナ患者では、コロナで亡くなったという死亡診断書を書いた人は一人もいない。
コロナと診断した人約450人全員に、診断直後から重症度に応じた治療を開始してきた。CTで肺炎があれば、すぐにステロイド剤やイベルメクチンを投与、血中酸素濃度が93%以下なら、その日のうちに在宅酸素を設置した。
医療が逼迫しているなら、ハイリスクの人が確実に入院できる体制を整え、軽症者は隔離期間とされる10日間、在宅の主治医をつけて自宅で管理するという方向性は間違っていない。
政府が、重症者や重症化リスクのある人以外は自宅療養を基本とするという方針を出し、最終的には「中等症以上は原則入院」となったが、「自宅療養」ではなく「在宅医療で治療します」と言うべき だった。
自宅療養の全員に在宅医をつけ、隔離する10日間は、24時間管理を保証して、薬も入院と同様に使えるようにすれば、入院しているのと変わらない医療を受けられ る。
提案① 5類に引き下げる。 ただし、医療費は5類になっても一定期間は公費負担を続ける。
3つのメリットがある。
・開業医による早期診断・即治療が可能=「早期発見、即治療」による重症化予防
・すぐに入院が必要な人は開業医が直接依頼(通常の病診連携)=タイムラグなし
・濃厚接触者の健康観察、入院先の割り振りが不要に=保健所崩壊解消
「5類にすれば全て氷解する。24時間医師と直接話せる体制、重症化リスクの高い人はドクター to ドクターで直接話せるような体制を構築することが大事」と する。
開業医による診断、治療について、次のように述べている。
現状は感染症法上は保健所が指揮を執る病気で、民間医が診てはいけないのかもしれないが、患者や家族から「入院できない。診てほしい」という電話がたくさんかかってくる。
医師には、医師法で定められた「応召義務」があるため、対応している。医師法第19条第1項 「診療に従事する医師は、診察治療の求があつた場合には、正当な事由がなければ、これを拒んではならない」
医療従事者は、民間に先立ってワクチンを受けている。コロナにかかる可能性、死亡する可能性は低い。
オンライン診療という方法もある。「5類」になった場合、治療をしないのは上記の医師法違反である。
提案② 現在、すぐに使える薬に「イベルメクチン」という特効薬がある。疥癬の治療で普段使っている薬。これを全国民に配る。
イベルメクチンの新型コロナウイルス感染症に対する臨床試験は世界各国で実施されている。
大村智博士がノーベル医学・生理学賞を受けた抗寄生虫薬の「イベルメクチン」がCOVID-19に効果があるとされている。アジアではその高い効果に注目が集まり、一部地域では需要が殺到している。東南アジア地域の一部医療関係者が「奇跡の治療薬」と称賛しているほどだと報じられている。
米国でもFDAはコロナ治療で利用を承認していないが、個人の選択において適応外使用が行われている。
日本では製造メーカーのMerck & Co., Inc.子会社 MSDが、腸管糞線虫症および疥癬用に商品名ストロメクトールで製造、マルホが販売する。
Merck & Co., Inc.は適応拡大に向けて動いていない。同社は2021年2月4日、イベルメクチンを新型コロナウイルス感染症治療に使う可能性について、データを検証したところ、安全性と効果は示されなかったと発表、寄生虫病の治療以外の用途で使用すべきでないと警告した。
そのなかで興和は、大村智特別栄誉教授より直接依頼を受け、本臨床試験実施を決断した。7月1日、新型コロナウイルス感染症患者を対象にイベルメクチンを投与する臨床試験を開始すると発表した。
2021/7/10 興和、新型コロナウイルス感染症患者を対象としたイベルメクチンの臨床試験を開始
中外製薬の「抗体カクテル療法」が承認され、初期の患者に効果があるが、供給量が限られている。
「これまで本人の承諾を得て100人くらいに投与している。治験中だがコロナ患者には適用外処方で使用できる。 最初の診断時に処方している。軽症者には非常によく効く。」
一般の病院では入手困難という。同クリニックは疥癬を扱っているため、入手できている。
(上記のMerck & Co., Inc.の警告を受け、MSDが供給を本来の目的に限定している可能性がある。)
「廉価で使えるイベルメクチンが広く行き渡る措置を取るように菅総理にもお願いしたい。『アベノマスク』のように、『スガノメクチン』(菅のメクチン)、『スガルメクチン』(メクチンに縋る)として国民全員に配布してほしい。」
ーーー
東京都医師会は8月13日、緊急の会見を開き、改めて感染対策の徹底を呼びかけた。
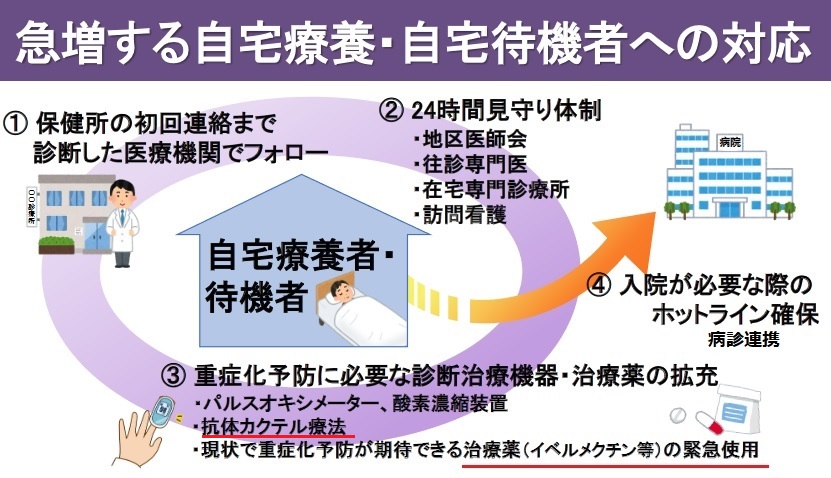
そのうえで、「保健所の機能がストップ状態に近くなっている」とし、自宅療養中の新型コロナウイルス感染者に対する診療体制を強化すると発表した。
東京都と連携し、保健所からの連絡が来るまでの間、診断した医療機関が健康観察を担う。往診専門医や訪問看護と連携した24時間の見守り体制を拡充する。
自宅に療養していて保健所などが医師の診察が必要だと判断した人について、オンラインで医師が診療する新たなシステムを導入する。
尾崎会長は「保健所の機能の肩代わりもやっていかざるをえないと思う。入院が必要と思った時に必ず入院や宿泊療養につなげられる仕組みをしっかり作っていきたい」と述べた。
発表資料は下記の通り。
保健所の機能不全を受けて、医療機関による自宅療養者の見守り、治療を実施するもので、特にイベルメクチンの効果を強調している。
尾崎治夫・東京都医師会会長は、BSフジ プライムニュースに長尾医師と一緒に出演しており、現時点で出来る範囲で(5類に変更せずでも出来る範囲で)長尾医師の主張(早期発見・即治療、病診連携、イベルメクチンの使用)を取り入れたと見られる。
付記 尾崎会長は9月7日の毎日新聞夕刊で以下のように述べている。
「コロナ医療で、使える薬を増やすことが大事。日本製ワクチンの開発にも期待しているけど、有効性が期待される既存の治療薬を日本でも使えるようにすべきだよ」。
例に挙げたのがイベルメクチンである。寄生虫によって失明するオンコセルカ症などの治療薬で、インドや南米ではコロナの治療薬として使われている。専門家の間ではコロナ治療への使用の賛否が割れ、日本ではまだ認められていないが、国内の製薬企業による臨床試験が近く始まる。
尾崎さんは「海外では実際に有効性を示すリポートも多数出ているし、治験に並行して現場で使えるような道も探っていきたい」との立場だ。
ーーー


最近のコメント